
Thema: EU
Europäische Kommission

Sartane: Risikobewertungsverfahren ist abgeschlossen
Pharmazeutische Unternehmer müssen zukünftig das Vorhandensein von NDMA- oder NDEA-Verunreinigungen in Sartanen ausschließen können. Allerdings erst nach einer Übergangsfrist von zwei Jahren. So ... » Weiterlesen

Fremanezumab: Migräne-Antikörper Nummer drei
Der Humanarzneimittelausschuss der EMA empfiehlt einen weiteren Antikörper zur Migräneprophylaxe zur Zulassung. Fremanezumab – Handelsname Ajovy® – ist nach Erenumab (Aimovig®) und ... » Weiterlesen

Harmloser Hanf?
Nicht jedes Produkt aus der Hanfpflanze (Cannabis sativa L.) ist für medizinische Zwecke bestimmt. Es gibt auch Erzeugnisse auf Hanfbasis, ohne Arzneimittelstatus, die als Lebensmittel, Nahrungsergä... » Weiterlesen
Gilenya erhält Zulassung für schubförmige MS bei Kindern
Der Markt therapeutisch zugelassener Arzneimittel bei pädiatrischen MS-Patienten ist überschaubar, vor allem bei hochaktiven Formen der multiplen Sklerose gibt es nichts. Das hat Novartis geändert... » Weiterlesen

Impfen gegen Migräne
Mit Erenumab (Aimovig®) ist ein neues Wirkprinzip zur vorbeugenden Behandlung der Migräne in den Behandlungsalltag eingezogen. Der monoklonale Antikörper bekämpft die Ursachen des Migrä... » Weiterlesen
Erste orale Therapie der Schlafkrankheit
Der Humanarzneimittelausschuss der EMA (CHMP) empfiehlt Fexinidazol zur Zulassung. Das Besondere: Fexinidazol von Sanofi ist das erste Arzneimittel, das oral und in beiden Stadien der durch ... » Weiterlesen
Galcanezumab: neuer Antikörper bei Migräne
Der Humanarzneimittelausschuss der EMA hat einen weiteren Antikörper bei episodischer und chronischer Migräne zur Zulassung empfohlen. Galcanezumab ist bereits der zweite CGRP-Antikörper, der zur ... » Weiterlesen
Wie findet der G-BA Ocrelizumab?
Mit Ocrelizumab, Ocrevus®, will Roche die Therapie der multiplen Sklerose revolutionieren. Es ist das erste Arzneimittel, das sowohl für die schubförmige multiple Sklerose (RMS), als auch für die ... » Weiterlesen

Präzisionswaffen zugelassen
cst | Mit der Zulassung von Tisagenlecleucel (Kymriah®) und Axicabtagen Ciloleucel (Yescarta®) durch die Europäische Kommission könnte eine Behandlung mit den Gentherapien bei bestimmten hä... » Weiterlesen

Gentherapie bei Leukämie: Novartis erhält EU-Zulassung für Kymriah
Am heutigen Montag hat die Europäische Kommission Kymriah® zur Behandlung der Leukämieformen ALL und DLBCL zugelassen. Bei der Gentherapie von Novartis handelt es sich um die erste CAR-T-Zell-... » Weiterlesen

EU genehmigt Phoenix Übernahme von Farmexim und Help Net
Die Übernahme der rumänischen Unternehmen Farmexim und Help Net Farma durch den Mannheimer Pharmahändler Phoenix Group ist endgültig in trockenen Tüchern: Die EU-Kommission hat ihre Zustimmung zu... » Weiterlesen
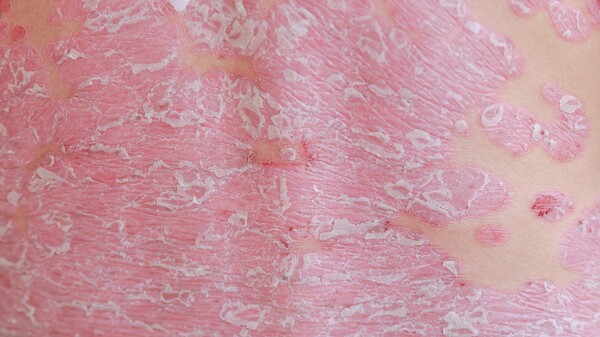
Tildrakizumab in der EU zur Zulassung empfohlen
16 Monate hat es gedauert, bis der CHMP Tildrakizumab von Almirall zur Zulassung empfohlen hat. Der Interleukin-23-Antikörper in Ilumetri® soll bei erwachsenen Patienten zur Behandlung ... » Weiterlesen

Orale Retinoide erhalten Warnbox
Das Risikobewertungsverfahren zu Retinoiden ist abgeschlossen, das BfArM setzt nun den Bescheid der Europäischen Kommission mit hoffentlich effektiveren Maßnahmen zur Schwangerschaftsverhütung um. ... » Weiterlesen

EMA untersucht Verunreinigung in valsartanhaltigen Arzneimitteln
Noch am gestrigen Donnerstag hat sich auch die Europäische Arzneimittelagentur in einer Pressemitteilung zu den EU-übergreifenden Valsartan-Rückrufen geäußert. Die EMA prüft gerade die Hintergr... » Weiterlesen

Zulassung für Denosumab erweitert
Zur Therapie einer Glucocorticoid-induzierten Osteoporose standen bislang nur einige wenige Wirkstoffe zur Verfügung. Mit Denosumab kommt nun eine neue, gut wirksame Therapieoption hinzu. Wie der ... » Weiterlesen

Gesunde Perspektiven
AMSTERDAM (diz) | Die Selbstmedikation wird in Zukunft mehr denn je ein zentraler Baustein sein für eine patientenorientierte, flächendeckende und finanzierbare Gesundheitsversorgung. Darauf machte ... » Weiterlesen

Erenumab in Europa zur Zulassung empfohlen
Im Mai 2018 erteilte die FDA Erenumab die Zulassung in den USA. Nun hat sich auch der CHMP bei der EMA positiv zum Migräne-Antikörper geäußert, Novartis rechnet noch in diesem Jahr mit dem ... » Weiterlesen

Ein unterschätztes Umweltgift?
Vergiftungen mit dem Schwermetall Blei können irreversible Schäden hinterlassen und sind bereits seit gut 2000 Jahren bekannt. Maler, die mit Blei-Farben malten, oder Arbeiter aus Blei-Minen ... » Weiterlesen

Trastuzumab-Biosimilar auf dem Markt
Im Februar hatte die Europäische Kommission die Zulassung für Herzuma® erteilt, seit Mai ist der monoklonale Antikörper Trastuzumab nun als Biosimilar in Deutschland verfügbar. Eingesetzt wird ... » Weiterlesen

Erstes Prasugrel-Generikum kommt von Mylan
Efient® bekommt generische Konkurrenz: Der CHMP bei der EMA hat Prasugrel® Mylan zur Zulassung empfohlen. Erteilt die Europäische Kommission diese, gewinnt Mylan das Rennen um das erste Prasugrel-... » Weiterlesen

Gehört Flupirtin wirklich auf den Müll?
rr | Der Pharmakovigilanz-Ausschuss (PRAC) der Europäischen Arzneimittelagentur (EMA) hat entschieden: Aufgrund des hepatotoxischen Potenzials ist es ratsam, die Zulassungen von Arzneimitteln mit dem... » Weiterlesen

Ein Flickenteppich von Höchstmengen und viel hilft nicht viel
„Viel hilft nicht viel und die EU soll (endlich) europäische Höchstgrenzen für Nahrungsergänzungsmittel definieren“ – das forderte der Bundesverband der Arzneimittel-Hersteller bei einem ... » Weiterlesen

„Alle EU-Bürger sollen sich gegen Grippe impfen lassen!“
Die Grippe hat Europa im Griff. Für Deutschland meldet das Robert-Koch-Institut unverändert eine stark erhöhte Influenza-Aktivität. 18.690 labordiagnostisch bestätigte Fälle wurden in der ... » Weiterlesen



















Foto: finecki / Fotolia