
Biopharmazeutika-Folgepräparate
Biosimilars

Pfizer darf Hospira unter Auflagen übernehmen
Die Europäische Kommission hat die von Pfizer geplante Übernahme des Spezialisten für injizierbare Medikamente und Infusionstechnologien Hospira geprüft und genehmigt. Die Genehmigung erfolgt ... » Weiterlesen

Biopharmazeutika im Aufwind
Biopharmazeutika – etwa monoklonale Antikörper, aber auch Impfstoffe – werden nach dem aktuellen Report der Boston Consulting Group (BCG) zur Medizinischen Biotechnologie in Deutschland ... » Weiterlesen

Nicht nur etwas für Auge und Ohr
MERAN (ck/du) | Die Veranstalter sprechen von einem Besucherrekord. Mehr als 800 Apothekerinnen und Apotheker haben am 53. Internationalen Fortbildungskongress der Bundesapothekerkammer in Meran ... » Weiterlesen

Mehr als nur ähnlich
Nach wie vor herrscht vor allem unter den Ärzten eine große Unsicherheit dahingehend, wie Biosimilars tatsächlich einzuschätzen sind. Der Grund liegt darin, dass die Zulassungssystematik für ... » Weiterlesen

Neue Arbeitsgemeinschaft „Pro Biosimilars“
Berlin - Deutschland hat nun auch eine eigene Interessenvertretung der Biosimilarunternehmen: Gestern gründete sich unter dem Dach des Branchenverbandes Pro Generika die Arbeitsgemeinschaft „Pro ... » Weiterlesen

Besondere Arzneimittelgruppen
Biologische Arzneimittel sind heute in der Behandlung zahlreicher schwerer Erkrankungen unverzichtbar. Das Spektrum umfasst immunologische Präparate wie Sera und Impfstoffe, Blutprodukte, ... » Weiterlesen
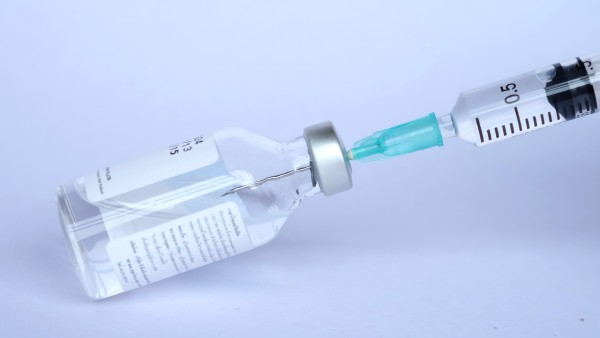
Erste Biosimilar-Zulassung erteilt
Remagen – Das Filgrastim-Biosimilar von Sandoz hat nun auch in den USA die Hürde der Nachahmer-Zulassung genommen und damit in den Vereinigten Staaten regulatorisches Neuland betreten. Die US-... » Weiterlesen

Der erste biosimilare Antikörper kommt
Die Markteinführung des ersten biosimilaren monoklonalen Antikörpers in wichtigen europäischen Ländern steht kurz bevor: Infliximab gibt es künftig auch von Hospira (Inflectra®) sowie von ... » Weiterlesen

Gleich, ähnlich oder anders?
Von Theo Dingermann und Ilse Zündorf | Nach Einführung der ersten Biopharmazeutika in den frühen Achtzigerjahren ist deren Bedeutung immer weiter gestiegen. Im Jahre 2012 stieg der Umsatz von ... » Weiterlesen

Remicade® = Inflectra® = Remsima®?
DAZ | Der Patentschutz des monoklonalen TNF-alfa-Antikörpers Infliximab (Remicade®) läuft zum 15. Februar 2015 aus. Ein schon 2013 von der EU zugelassenes Biosimilar, entwickelt von der ... » Weiterlesen

Erstes Humira-Biosimilar weltweit
Zydus Cadila, nach Marktanteilen der viertgrößte indische Arzneimittelhersteller, hat auf dem heimischen Markt das erste Biosimilar zu Humira unter dem Namen Exemptia gelaunched. Das Originalprä... » Weiterlesen

Stada schielt auf Humira-Biosimilar
Die Stada Arzneimittel AG und der Biotechspezialist mAbxience wollen über die Einlizenzierung eines Biosimilars zu Adalimumab (Humira) verhandeln. Wie Stada mitteilt, haben die Unternehmen vereinbart... » Weiterlesen

EMA pusht Biosimilars
REMAGEN (hb) | Die Europäische Arzneimittelagentur (EMA) hat ihre Rahmenrichtlinie für Biosimilars geändert. Danach dürfen Antragsteller, die Biosimilars entwickeln, in bestimmten klinischen ... » Weiterlesen

EMA will weltweite Biosimilar-Entwicklung pushen
Die Europäische Arzneimittelagentur hat in ihrer Rahmenrichtlinie für Biosimilars eine wichtige Änderung eingeführt. Nach der jetzt veröffentlichten revidierten Guideline dürfen Antragsteller, ... » Weiterlesen

Pro Generika fordert fairen Wettbewerb
Für zwei Drittel aller GKV-Versicherten bestehen im Fall der Fälle Rabattverträge über das Original-Biopharmazeutikum Remicade®. Der Branchenverband Pro Generika sieht dies kritisch. Schließlich... » Weiterlesen

Biosimilars in den Startlöchern
BERLIN (ks) | Im kommenden Jahr werden eine Reihe Biopharmazeutika ihren Patentschutz verlieren – unter anderem die kostenintensiven Arzneimittel Humira® und Lantus®. Erste Biosimilars dieser Prä... » Weiterlesen

Biosimilars den Weg bereiten
Im kommenden Jahr wird eine Reihe Biopharmazeutika ihren Patentschutz verlieren – etwa die kostenintensiven Arzneimittel Humira® und Lantus®. Erste Biosimilars warten bereits auf den Markteintritt... » Weiterlesen

Erstes Insulin-Biosimilar in Europa zugelassen
Die Europäische Kommision hat dem ersten Insulin-Biosimilar die Zulassung für Europa erteilt: LY2963016 Insulin glargin ist ein Basalinsulin, das die gleiche Aminosäuresequenz wie Lantus® hat. Auf... » Weiterlesen

Zweifel an der Austauschbarkeit
Im Juli 2013 wurde in der EU das erste Biosimilar des monoklonalen Antikörpers (mAb) Infliximab (Inflectra, Remsima) für die gleichen Indikationen wie das Originalpräparat Remicade zugelassen – ... » Weiterlesen

Kommission stellt Kartellrechts-Untersuchung ein
Die EU-Kommission hat die kartellrechtliche Untersuchung zu in Frankreich tätigen Generikaherstellern eingestellt. Anlass der Untersuchung waren Vermutungen, dass sich die Generikaunternehmen in ... » Weiterlesen

Die Ruhe vor dem Sturm?
Biopharmazeutika gehören heute bei zahlreichen schweren Erkrankungen zum unverzichtbaren Handwerkzeug der modernen Medizin. Da sie teurer sind als kleinmolekulare Arzneimittel, sind Nachahmer-... » Weiterlesen

CHMP empfiehlt Zulassung von neuem Insulin glargin-Produkt
Der europäische Ausschuss für Humanarzneimittel (CHMP) hat eine Empfehlung zur EU-weiten Zulassung des Insulin glargin-Produktes LY2963016 zur Behandlung von Typ-1- und Typ-2-Diabetes ausgesprochen... » Weiterlesen

„Dramatische Entwicklung“
BERLIN (ks) | Generika schrieben in den letzten Jahren Erfolgsgeschichte. Sie sind heute aus dem Versorgungsalltag nicht mehr wegzudenken. Vor allem die Krankenkassen schätzen die günstigen ... » Weiterlesen
















juustright / stock.adobe.com