
Thema
Committee for Medicinal Products for Human Use
Remdesivir bald in Europa?
Gilead hat nun auch bei der Europäischen Arzneimittel-Agentur EMA die Zulassung für Remdesivir eingereicht. Der RNA-Polymerasehemmer war das erste zugelassene Arzneimittel bei COVID-19, in den ... » Weiterlesen
Mit zwei neuen Impfstoffen gegen Ebola
Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur hat empfohlen, die von Janssen Pharmaceuticals entwickelte Impfstoffkombination aus Zabdeno (Ad26.ZEBOV) und ... » Weiterlesen
Sollten sich Ältere mit Fluad Tetra oder Efluelda gegen Grippe impfen lassen?
Bei älteren Menschen wirkt eine saisonale Grippeimpfung meist schlechter als bei Jüngeren, gerade Ältere erkranken jedoch häufiger besonders schwer an Influenza und versterben. Was tun? Es gibt ... » Weiterlesen

Keine vorschnelle Remdesivir-Zulassung
Remdesivir ist in den USA bereits genehmigt. Die EMA erlaubt das erste COVID-19-Arzneimittel nur in klinischen Studien oder Härtefallprogrammen, kündigte jedoch jüngst die baldige Zulassung an. ... » Weiterlesen
Efluelda – hochdosiert für ältere Menschen
Ältere Menschen entwickeln besonders häufig schwere Grippeverläufe mit Komplikationen wie Pneumonie. Gerade bei Älteren wirkt jedoch die Influenzaimpfung meist weniger gut als bei Jüngeren. ... » Weiterlesen

EU plant bedingte Marktzulassung für Remdesivir
cel | Die Europäische Arzneimittel-Agentur (EMA) plant kurzfristig die bedingte Marktzulassung von Remdesivir für die Behandlung von COVID-19-Patienten. Dies erklärte der Direktor der Europä... » Weiterlesen
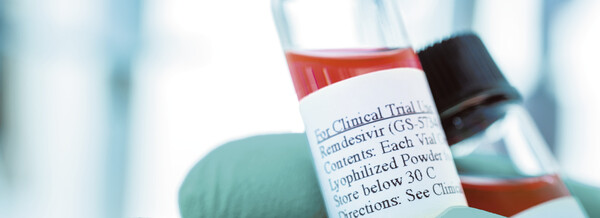
Warten auf Evidenz
Derzeit konzentriert sich die Forschung zu Pharmaka gegen COVID-19 hauptsächlich auf Arzneimittel, die schon gegen andere Krankheiten zugelassen oder zumindest in der Entwicklung sind. Bei diesem „... » Weiterlesen

Breiterer Einsatz von Remdesivir
cel/ral | Remdesivir wird in der EU bislang nur im Rahmen von Härtefallprogrammen (Compassionate Use) eingesetzt, und zwar nur bei COVID-19-Patienten, die eine invasive maschinelle Beatmung benö... » Weiterlesen
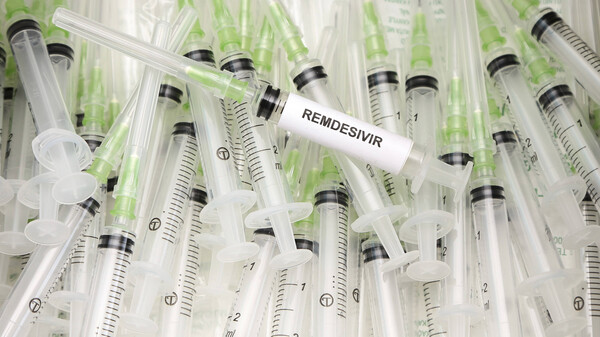
Compassionate Use: Mehr Coronapatienten erhalten Remdesivir
In den Vereinigten Staaten ist Remdesivir bereits zugelassen, auch Japan setzt das Virostatikum bei COVID-19 seit Kurzem offiziell ein. Nun zieht die Europäische Arzneimittel-Agentur nach, zwar nicht... » Weiterlesen

Notfallgenehmigung für Remdesivir
cel | Remdesivir ist zur COVID-19-Behandlung zugelassen – bislang nur durch die FDA in den USA und nur in Form einer Notfallgenehmigung. Das Virostatikum soll laut einer Studie in den USA die ... » Weiterlesen
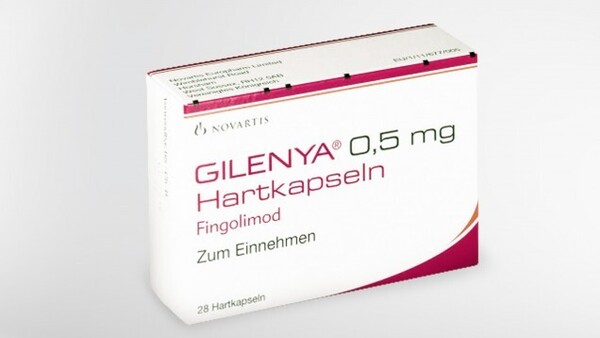
Gilenya wird generisch, Novorapid bekommt Biosimilar-Konkurrenz
Das zur Behandlung einer hoch aktiven remittierend-schubförmigen Multiplen Sklerose eingesetzte orale Arzneimittel Gilenya bekommt generische Konkurrenz: Am 30. April 2020 empfahl der Ausschuss für ... » Weiterlesen
CHMP empfiehlt erste fixe Dreierkombination für Asthmatiker
Der Humanarzeimittelausschuss der Europäischen Arzneimittel-Agentur empfiehlt die erste einmal täglich anzuwendende fixe Dreierkombination bei Asthma – Enerzair-Breezhaler mit Indacaterol, ... » Weiterlesen
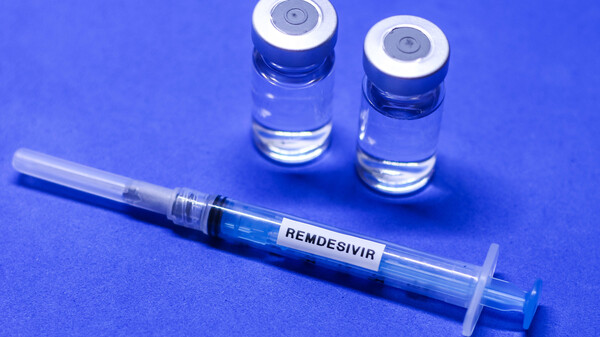
EMA prüft Remdesivir
Remdesivir ist zugelassen – bislang nur durch die FDA in den Vereinigten Staaten und nur in Form einer Notfallgenehmigung, die keiner formellen Zulassung entspricht. Das Virostatikum soll laut einer... » Weiterlesen
Grippeimpfstoff Fluad wird vierfach
Der Humanarzneimittelausschuss der Europäischen Arzneimittel-Agentur EMA hat Ende März einen neuen Grippeimpfstoff zur Zulassung empfohlen: Fluad Tetra – noch nie dagewesen ist Fluad aber nicht. ... » Weiterlesen

Fosfomycin neu bewertet
mp | Das Antibiotikum Fosfomycin wird sowohl oral als auch parenteral zur Behandlung verschiedener Infektionen eingesetzt. Da sich das Resistenzprofil in den letzten Jahrzehnten kaum geändert hat, ... » Weiterlesen
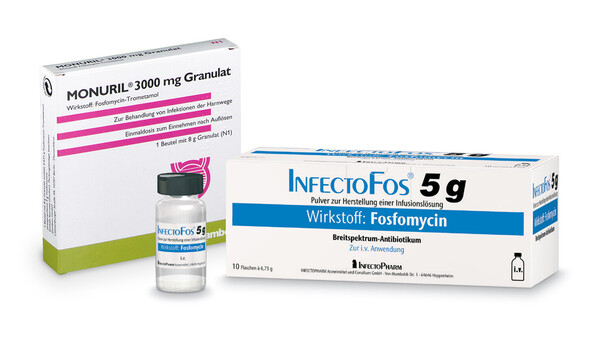
EMA beschränkt Anwendung von Fosfomycin
Die Anwendung des Antibiotikums Fosfomycin soll eingeschränkt werden. Seit Dezember 2018 hatte der CHMP der EMA Nutzen und Risiken von Fosfomycin überprüft – unter anderem oral bei ... » Weiterlesen

Methocarbamol + Paracetamol: Kombination bei Rückenschmerzen sinnvoll?
Ein Arzneimittel gegen die Schmerzen und etwas zur Muskelentspannung – das klingt gegen Rückenschmerzen nach einer plausiblen Therapie-Kombination, oder? In Spanien wird eine solche ... » Weiterlesen

Zolgensma in der EU zur Zulassung empfohlen
Der Humanarzneimittelausschuss der EMA empfiehlt, Zolgensma auch in der EU zuzulassen. Das Gentherapeutikum zur Behandlung schwerer Formen der Spinalen Muskelatrophie gilt mit etwa zwei Millionen ... » Weiterlesen
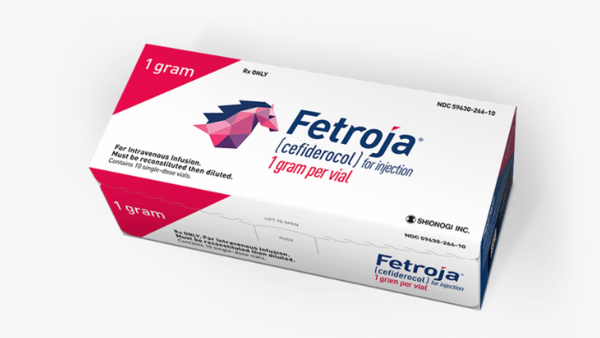
Cefiderocol: Antibiotikum als trojanisches Pferd
Der Humanarzneimittelausschuss der EMA empfiehlt das Cephalosporin Cefiderocol zur Zulassung. Fetroja wirkt gegen aerobe gramnegative Erreger und trickst als Siderophor-Cephalosporin gängige ... » Weiterlesen

Vorerst kein Galcanezumab bei Clusterkopfschmerz
Der CHMP ist nicht überzeugt: Der Humanarzneimittelausschuss der EMA versagte Lilly die Zulassungsempfehlung für Galcanezumab zur Prävention bei Erwachsenen mit Clusterkopfschmerz. Die Europäische... » Weiterlesen


















Foto: dpa