Was ist die Westafrikanische Schlafkrankheit?
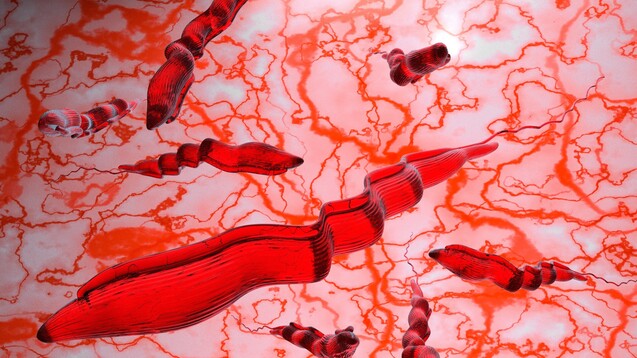
Die Westafrikanische Schlafkrankheit wird medizinisch korrekt als Humane Afrikanische Trypanosomiasis (HAT) bezeichnet. Man unterscheidet zwei Arten der Schlafkrankheit abhängig davon, welcher Parasit ursächlich ist: Trypanosoma brucei gambiense oder Trypanosoma brucei rhodensiense, wobei 98 Prozent der gemeldeten Fälle durch Trypanosoma brucei gambiense verursacht werden.
Trypanosoma brucei gambiense ist vor allem in den tropischen Ländern West- und Zentralafrikas verbreitet. Die meisten Fälle finden sich in der Demokratischen Republik Kongo. In Ostafrika bis südwärts nach Botswana dominiert Trypanosoma brucei rhodensiense. 25 Prozent der Erkrankten sind Kinder unter 15 Jahren.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.