
- DAZ.online
- News
- Spektrum
- Neue Schnelldiagnostik zu...
EU-finanziertes Forschungsprojekt
Neue Schnelldiagnostik zu COVID-19
Remagen - 08.06.2020, 16:15 Uhr
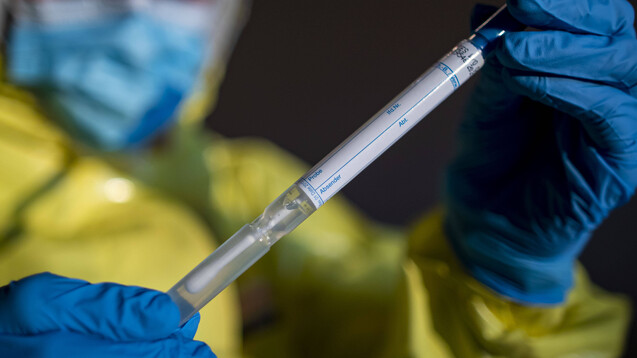
Die irische Firma Hibergene hat einen Coronavirus-Test entwickelt, der innerhalb von 30 Minuten nach einem Abstrich ein Ergebnis liefern soll. Das Projekt wird mit EU-Forschungsgeldern unterstützt. (x / Foto: imago images / Reichwein)
Irische Wissenschaftler haben die Genehmigung erhalten, einen neuen Schnelltest für COVID-19 auf den Markt zu bringen. Das tragbare Diagnosesystem soll eine bestehende Infektion innerhalb von 30 Minuten zuverlässig anzeigen können.
Der irische Hersteller HiberGene Diagnostics hat die CE-Zertifizierung für einen neuen Schnelltest auf SARS-CoV-2 erhalten. Darüber freut sich nicht nur das Unternehmen, sondern auch die Europäische Kommission, denn die EU hat das Projekt HG nCoV19-Test, an dem öffentliche und private Organisationen aus Irland, Italien, Großbritannien und China beteiligt sind, mit 930.000 Euro bezuschusst.
Einfach, schnell und genau
Nach Angaben von HiberGene verwendet der neue COVID-19-Test dessen firmeneigenes gefriergetrocknetes molekulares Reagenzienformat, das einfach zu handhaben sein soll. Das virale Genmaterial wird mit Hilfe der Schleifen-vermittelten isothermen Amplifikation (LAMP) vervielfältigt. Als Probenmaterial dienen Nasen-/Rachenabstriche. Mit dem kleinen tragbaren HG Swift-Instrument können vier Proben gleichzeitig getestet werden.
Bei Proben mit hoher bis mäßiger Viruslast soll die Detektion zuverlässig sein, wobei positive Ergebnisse im Durchschnitt innerhalb von 30 Minuten zu erwarten sind. Dies soll eine schnelle Diagnose der Krankheit im frühen und hochinfektiösen Stadium ermöglichen. Negative Befunde sollen innerhalb von 60 Minuten verfügbar sein. Das System besitze eine Empfindlichkeit, die der der aktuellen PCR-Systeme für Proben in allen Stadien der COVID-19-Infektion entspreche, erklärt das Unternehmen.
Studien zum erweiterten Einsatz geplant
Die Wirksamkeit des Tests wurde nach Angaben von HiberGene über eine klinische Evaluierungsstudie am Mater Private Hospital in Dublin nachgewiesen. Weitere Studien zur Bewertung eines erweiterten Einsatzes, etwa zur Kompatibilität mit neuen Probenarten und Patientenkohorten, einschließlich klinischer Bewertungen sind geplant. Als Partner in dem Projekt werden das zum Universitätsklinikum von Genua gehörende IRCCS Ospedale Policlinico San Martino in Italien, die Queens University in Belfast, Nordirland, und der chinesische Vertriebspartner von HiberGene, Medcaptain Medical Technologies, genannt.
Das neue COVID-19-Diagnostikum soll jetzt in Irland und international zum Verkauf angeboten werden. „Der Test eignet sich sowohl für dezentrale Einrichtungen, die schnelle molekulare Tests für Screenings benötigen, als auch für zentralisierte Labore, die zusätzliche Testungen zur Bestätigung oder Tests außerhalb der Geschäftszeiten brauchen“, erläutert Seamus Gorman, CEO von HiberGene.
Drei Projekte zu COVID-19-Diagnostika in der Förderung
„Dies ist ein großartiges Beispiel für die EU-Forschung in Aktion“, erklärt Mariya Gabriel, EU-Kommissarin für Innovation, Forschung, Kultur, Bildung und Jugend. „Es macht Mut zu sehen, dass die Forscher sich der Herausforderung gestellt und dieses neue Diagnosesystem so schnell entwickelt und damit eines der Ziele unseres ersten Aufrufs erreicht haben.“
Gabriel bezieht sich mit dieser Äußerung auf einen Aufruf zur Interessenbekundung für eine finanzielle Förderung mit dem Titel „SC1-PHE-CORONAVIRUS-2020“, die die Kommission bereits am 30. Januar 2020 veröffentlicht hatte. Mittlerweile fördert die EU insgesamt 18 Projekte zu epidemiologischen Fragestellungen sowie zu Entwicklung von Schnelldiagnostika, Behandlungen und Impfstoffen zu COVID-19, an denen 140 Forschungsteams beteiligt sind. Das Budget dafür aus dem EU-Forschungs- und Innovationsprogramm Horizon 2020 wird mit 48,5 Millionen Euro beziffert.
Das HiberGene-Projekt ist eines von dreien, die sich mit der Entwicklung von Schnell-/Point of Care-Diagnostika befassen. Es war erst Ende März in die Förderung gekommen und sollte den Schwerpunkt auf die Diagnose in frühen Stadien der Erkrankung legen.
Ein weiteres Projekt mit der Bezeichnung CoNVat unter der Leitung eines spanischen Instituts für Nanowissenschaften und Nanotechnologie soll Nanobiosensing Plattformen für Point of Care-Tests entwickeln und CoronaDX, das von der technischen Universität Dänemark koordiniert wird, widmet sich ebenfalls drei Point-of Care-Schnelldiagnostika.

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.