
- DAZ.online
- News
- Pharmazie
- USA genehmigen Comirnaty ...
Pfizer/Biontech-Impfstoff
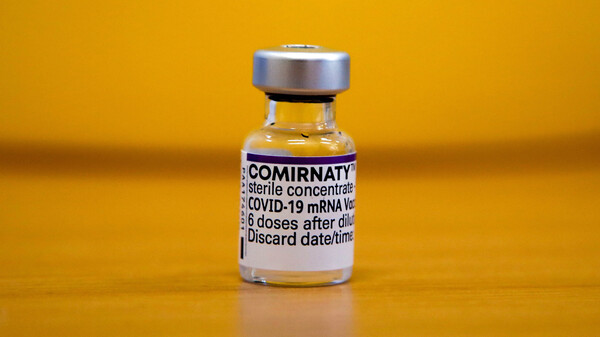
USA genehmigen Comirnaty für Kinder ab fünf Jahren
Stuttgart - 01.11.2021, 12:15 Uhr
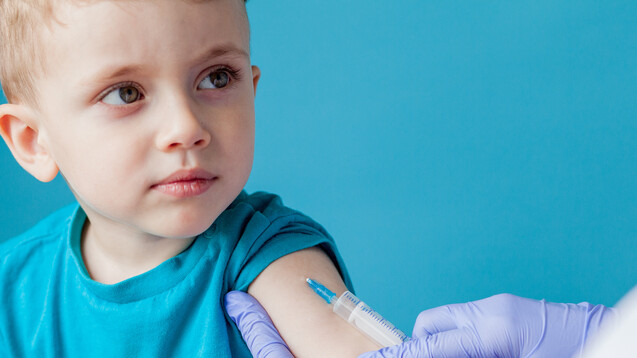
Die US-amerikanische Arzneimittelbehörde FDA erteilte Comirnaty®, dem COVID-19-Impfstoff von Pfizer/Biontech, am 29. Oktober die Notfallzulassung für die Impfung bei Kindern im Alter zwischen fünf und elf Jahren. (s / Foto: volody10 / AdobeStock)
Myokarditis bei Kindern
Dem Risiko einer Myokarditis (Herzmuskelentzündung) und Perikarditis (Herzbeutelentzündung) nach Pfizer/Biontech-Impfung widmete die FDA eine separate Risiko-Nutzen-Bewertung. Myo- und Perikarditiden nach Impfung mit mRNA-Impfstoffen betreffen aktuellen Kenntnissen zufolge vor allem junge Männer (laut FDA beobachtet man die höchste Rate bei 12- bis 17-Jährigen) und eher die zweite Impfdosis als die erste. In Deutschland informierten Pfizer/Biontech (und Moderna) im Juli in einem Rote-Hand-Brief über das Risiko von Herzmuskelentzündungen. In einem Modell verglich die FDA nun, wie viele Krankenhausaufenthalte, Intensivbehandlungen und Todesfälle sich durch COVID-19-Impfung von Kindern verhindern ließen, mit Myokarditis-Fällen, Krankenhausaufenthalten, Intensivbehandlungen und Todesfällen, die Comirnaty® im Gegenzug verursachen könnte. Das Fazit der FDA: Im Modell überwiegen die Vorteile der Impfung deren Risiken.
Warum analysierte die FDA nicht die Zahl der Myokarditisfälle aus der Studie? Die Teilnehmerzahl ist mit 4.600 Kindern zu klein, um Aussagen treffen zu können. So kommt es laut dem Sicherheitsbericht des Paul-Ehrlich-Instituts vom 26. Oktober bei 12- bis 17-jährigen männlichen Jugendlichen zu 4,81 Fällen einer Myokarditis auf 100.000 Impfdosen. In der Sicherheitsstudie mit 4.600 Kindern wurden jedoch deutlich weniger als ein Zehntel dieser Impfdosen (unter 10.000) appliziert, wodurch statistisch betrachtet weniger als 0,48 Kinder eine Myokarditis entwickeln würden.
Auch EMA prüft Comirnaty bereits bei Kindern
Auch die EMA prüft bereits die von Pfizer/Biontech eingereichten Daten zu Comirnaty® für eine bedingte Zulassung des COVID-19-Impfstoffs bei Kindern zwischen fünf und elf Jahren. Und auch die Konkurrenz schläft nicht: Moderna gab vor wenigen Tagen positive Studienergebnisse zu seinem COVID-19-Impfstoff Spikevax® bei Kindern zwischen sechs und elf Jahren bekannt und die Absicht, die Zulassung bei FDA, EMA und weiteren Arzneimittelbehörden weltweit einzureichen.
Mehr zum Thema

Moderna plant Zulassung
Robuste Antikörperantwort auch bei 6-jährigen Kindern
Wie die FDA berichtet, machen in den USA die COVID-19-Fälle bei Kindern im Alter von fünf bis elf Jahren 39 Prozent der Fälle bei unter 18-Jährigen aus, und etwa 8.300 Kinder mussten deswegen im Krankenhaus behandelt werden. Bis zum 17. Oktober sind laut FDA 146 Kinder zwischen fünf und elf im Zusammenhang mit einer COVID-19-Erkrankung verstorben.























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.