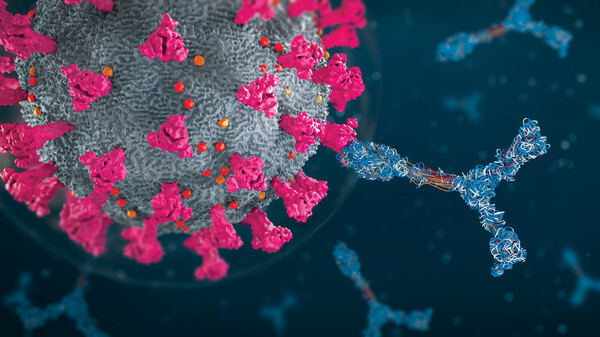
Mit Blick auf eine vierte Welle, die nach seiner Einschätzung auch in den Krankenhäusern spürbar werden dürfte, sei man an der Charité froh, dass die Präparate zur Verfügung stehen, sagte Suttorp. Man müsse damit rechnen, dass das Virus im Herbst zunächst in den Schulen um sich greife und es wieder zu Ansteckungen in Familien kommen könne – etwa der Großeltern. Denn bisherige Erkenntnisse ließen eine nachlassende Impfwirkung bei älteren Menschen befürchten. Hinzu kommt, dass die Delta-Variante deutlich ansteckender ist als frühere Formen. Als Kombinationstherapie könnten die Antikörper auch gegen Delta eingesetzt werden, sagte Suttorp. Wenn die Atikörpertherapien sich in der Praxis also nützlich erweisen, ist dann wirklich bald mit einer Zulassung in Deutschland zu rechnen?
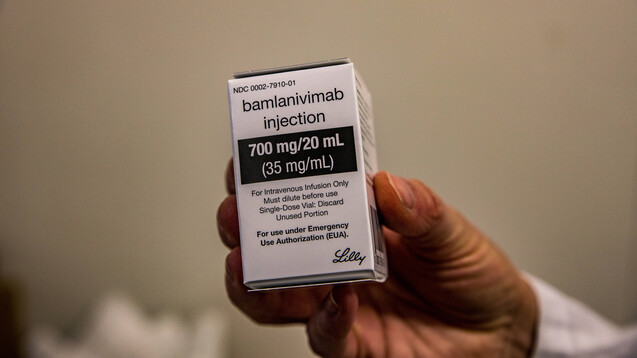
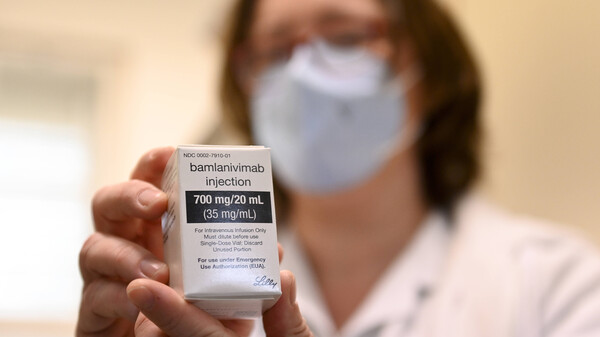
Wie das Bundesgesundheitsministerium auf Anfrage der dpa mitteilte, wird mit ersten Zulassungen durch die Europäische Kommission noch im dritten Quartal 2021 gerechnet. Mit Stand 16. Juli seien insgesamt rund 3.600 Einheiten solcher Arzneimittel abgegeben worden, hieß es vom Ministerium. Erste Rückmeldungen aus der Anwendungspraxis seien positiv. Begleitende Studien zum „notfallmäßigen Einsatz“ seien seitens des Ministeriums jedoch nicht vorgesehen. Die monoklonalen Antikörper sind den Angaben nach teils bis Herbst 2021 haltbar, teils aber auch deutlich länger.



























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.