
- DAZ.online
- News
- Recht
- Schadenersatzprozess ...
Sammelklage in Frankreich
Schadenersatzprozess gegen Merck beginnt
München - 03.12.2018, 17:50 Uhr
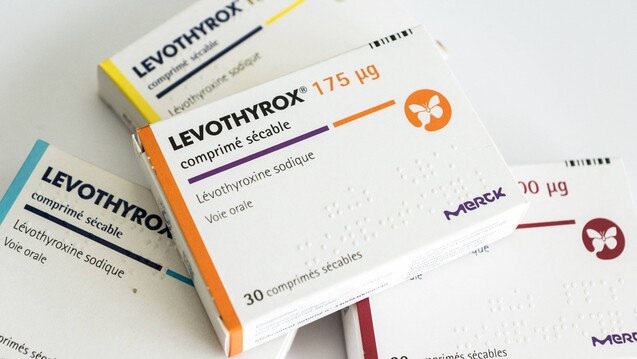
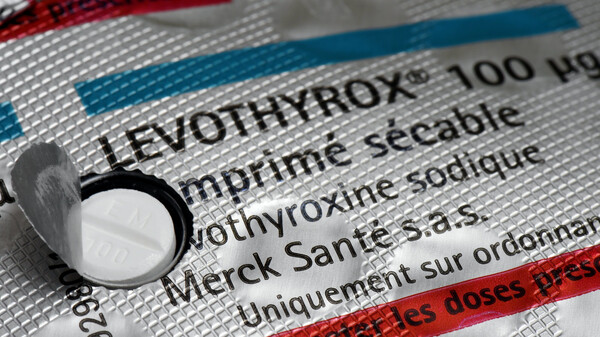
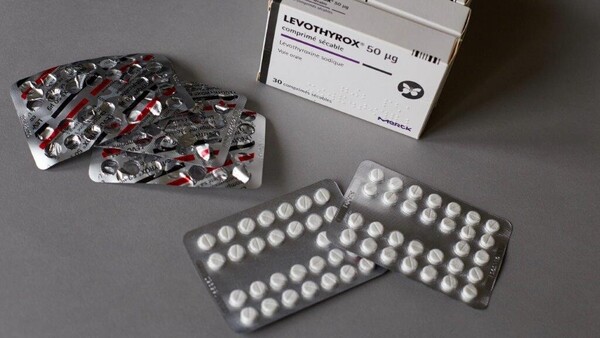
Wie in Frankreich Levothyrox, soll auch in Deutschland Euthyrox in neuer Formulierung voraussichtlich im zweiten Quartal 2019 in die Apotheken kommen. (Foto: ZUMA Press / imago)
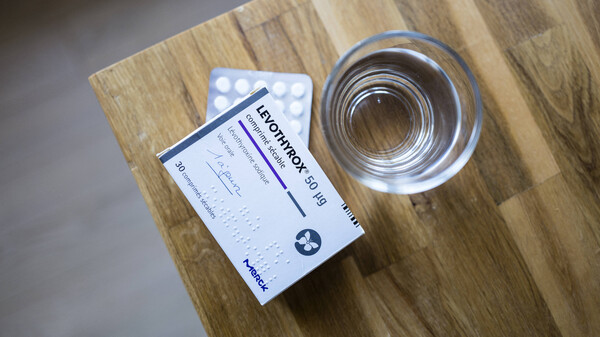
Der Darmstädter Pharma- und Chemiekonzern Merck ist seit dem heutigen Montag in Frankreich mit einem Zivilprozess konfrontiert. Patienten hatten sich über unerwünschte Nebenwirkungen der im Frühjahr 2017 in Frankreich eingeführten neuen Rezeptur des Schilddrüsenmittels Levothyrox beschwert – in anderen Ländern unter dem Namen Euthyrox oder Eutirox im Handel. In dem Zivilprozess in Villeurbanne bei Lyon fordern die Kläger nun in einer Sammelklage Schadenersatz.
Nach einem Bericht der Nachrichtenagentur dpa-AFX haben sich mehr als 4100 Kläger der Sammelklage angeschlossen. Sie würden jeweils 10.000 Euro Schadenersatz fordern. Merck hatte die neue Zusammensetzung auf Bitten verschiedener internationaler Gesundheitsbehörden, darunter auch der französischen Medikamentenbehörde ANSM, entwickelt.
In den Monaten nach der Umstellung meldeten zahlreiche Patienten Nebenwirkungen. Die Kläger in Villeurbanne werfen dem Pharmahersteller laut dpa-AFX nun vor, nicht ausreichend über die veränderte Rezeptur und mögliche Auswirkungen informiert zu haben. Merck wiederum weist die Vorwürfe auf Anfrage von DAZ.online zurück: „Merck lehnt die von den Anwälten der Kläger erhobenen Ansprüche entschieden ab und weist ausdrücklich darauf hin, dass die Qualität der neuen Zusammensetzung von Euthyrox® (Lévothyrox® in Frankreich) bereits mehrmals bestätigt worden ist. Darüber hinaus erlauben wir uns den Hinweis, dass die Informationen, die Ärzte, Apotheker und Patientengruppen zu der Einführung dieser neuen Zusammensetzung erhalten haben, im Rahmen der geltenden französischen Vorschriften vorbildlich waren.“
Mehr zum Thema
Merck formuliert Schilddrüsenmedikament neu
Euthyrox-Rezeptur ändert sich
Laut dpa-AFX argumentiere der Konzern zudem damit, dass das Gericht in Lyon nicht zuständig sei. Der Anwalt des Unternehmens habe gefordert, den Fall an ein höheres Gericht, das Tribunal de Grande Instance, zu verweisen – nur dort könne über Fälle von Körperverletzung in diesem Ausmaß entschieden werden.
Die Zivilklage der Levothyrox®-Patienten in Lyon zielt nach Angaben der Nachrichtenagentur allerdings nicht auf Körperverletzung, sondern auf „fehlende Information“ und „Schaden durch Angst“ ab, weil die Patienten nicht gewusst hätten, weshalb sie plötzlich gesundheitliche Probleme gehabt hätten.
Euthyrox vor Einführung in Deutschland
Die Thematik könnte nicht nur auf Frankreich beschränkt bleiben. Im Juli dieses Jahres hatte Merck mitgeteilt, dass das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) empfohlen hat, die neue Formulierung von Euthyrox® im Rahmen des EU-Zulassungsprozesses in 21 EU-Ländern, darunter auch in Deutschland, zu genehmigen. Die nationalen Zulassungen würden nach dieser Empfehlung erteilt. Eine Merck-Sprecherin bestätigte gegenüber DAZ.online, dass die Arznei in neuer Formulierung hierzulande voraussichtlich im zweiten Quartal 2019 in die Apotheken kommen soll.
Die engere Spezifikation des Wirkstoffs in der neuen Formulierung hat zum Ziel, Patienten eine bessere Kontrolle über ihre individuelle Dosierung von Levothyroxin® zu ermöglichen, so Merck im vergangenen Sommer. Die Empfehlung des BfArM basiere auf einer Studie, die die Bioäquivalenz zwischen der ursprünglichen und der neuen Zusammensetzung belegt.
Nach Einschätzung der Schilddrüsenliga seien alle Patienten, die Euthyrox® nehmen, denselben Risiken ausgesetzt wie die Patienten in Frankreich. Nach anderen Berichten sollen auch einzelne Patienten in der Schweiz, wo das neue Euthyrox® bereits das alte Präparat abgelöst hat, Problemen durch die Umstellung haben. Allerdings seien diese weniger gravierend als in Frankreich, da es in der Schweiz ebenso wie in Deutschland eine große Auswahl an alternativen Präparaten und damit weniger Betroffene gebe.
Mehr zum Thema
Warum Deutschland auf ein geändertes Euthyrox® vorbereitet sein sollte
Stabil, aber unverträglich?

Interview mit Prof. Dr. Henning Blume
„Rezeptur-Umstellung ist zwingend erforderlich“
Merck weist seinerseits darauf hin, dass bei
Schilddrüsenarzneimitteln kleinste Dosisvariationen das
Schilddrüsengleichgewicht der Patienten beeinflussen können. Behandelnden
Ärzten werde daher empfohlen, die Patienten bei der Verschreibung der neuen
Formulierung genau zu beobachten.
Euthyrox® wird angewendet zur Therapie eines gutartigen Kropfes bei
Patienten mit normaler Schilddrüsenfunktion, zur Verhütung einer erneuten
Kropfbildung nach Operation, als Ersatz für das natürliche Schilddrüsenhormon,
bei Schilddrüsenüber- und -unterfunktion und zur Unterdrückung erneuten
Tumorwachstums bei Patienten mit Schilddrüsenkrebs.



















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.