
- DAZ.online
- News
- Pharmazie
- Eine lukrative Geldquelle...
Orphan Drugs
Eine lukrative Geldquelle?
Remagen - 07.10.2016, 17:00 Uhr

Vergoldet sich die Pharmaindustrie seltene Erkrankungen? (Sondem / Fotolia)
Das
Handelsblatt und das ARD-Magazin Plusminus haben diese Woche Arzneimittel gegen seltene
Erkrankungen (Orphans Drugs) aufs Korn genommen. „Der Milliarden Trick“ titelte
das Handelsblatt provokant und attackierte damit die Pharmaindustrie, die die
seltenen Krankheiten als lukrative Geldquelle entdeckt haben soll.
Rund ein Fünftel der Medikamente, die jährlich neu auf den Markt kommen, sind sogenannte Orphan Drugs. Die Unternehmen entsprächen damit den Forderungen von Patienten und Selbsthilfegruppen, Ärzten, Politik und der EU-Kommission nach verstärktem Engagement auf diesem Gebiet, stellt der Verband der forschenden Pharma-Unternehmen (vfa) fest. In der Tat ist die Entwicklung von Arzneimitteln für seltene Erkrankungen sowohl in der EU wie auch jenseits des Atlantiks in den USA gesundheitspolitisch hoch aufgehängt.
Nur ein Prozent behandelbar
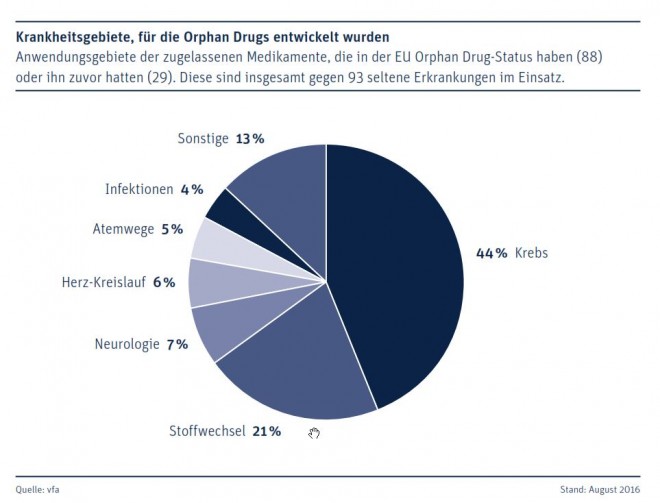
Erst mit Inkrafttreten der entsprechenden EU-Verordnung im Jahr 2000 hatte der Sektor etwas Fahrt aufgenommen. Trotzdem fristen die Präparate zahlenmäßig gemessen am Umfang der Betroffenen (rund 30 Millionen Menschen in der EU) und der Anzahl der einzelnen Erkrankungen immer noch ein Nischendasein. Derzeit sind nach Angaben des Bundesverbandes der Pharmazeutischen Industrie (BPI) nur etwa ein Prozent der rund 8.000 seltenen Erkrankungen medikamentös behandelbar. Die Medikamente, die in der EU den Orphan Drug-Status haben (88) oder ihn zuvor hatten (29) richten nach vfa-Angaben gegen insgesamt 93 seltene Erkrankungen.
Nichts gegen das Fragile-X-Syndrom?
Dennoch
stehen Orphan Drugs immer wieder in der Kritik. Diese Woche haben sich nach
gemeinsamer Recherche das Handelsblatt und das ARD-Magazin Plusminus des Themas
angenommen. Ihr Bespiel: Zwei Jungen aus Hamburg, die an dem Fragilen X-Syndrom
leiden, einer seltenen Krankheit, die zu autistischen Verhaltensweisen führt.
Bislang habe die Pharmaindustrie wenig Interesse gezeigt, Geld in die Suche
nach einem Mittel dagegen zu stecken, wird behauptet. Der vfa verweist im
Gegenzug darauf, dass bereits sieben Wirkstoffe gegen das seltene
Fragile-X-Syndrom den Orphan Drug-Status erhalten hätten, die sich jedoch alle
noch in der Erprobung befänden.
Zu Recht viele Vergünstigungen?
Im Handelsblatt heißt es weiter, in den USA und der EU seien massiv Anreize für Unternehmen geschaffen worden, an seltenen Krankheiten zu forschen. Die Vorteile reichten von geringeren Zulassungsgebühren über Steuervorteile bis hin zu einer langjährigen Marktexklusivität für Orphan Drugs. Dies trifft zu und war politisch ausdrücklich gewollt, denn ansonsten hätte es auf diesem Gebiet wohl kaum die Fortschritte gegeben, von denen die Orphan-Patienten heute bereits profitieren können. Über die Zulassung hinaus behält das Medikament den Orphan-Drug-Status übrigens nur, wenn es sich als bisherigen Therapien überlegen erwiesen hat, also einen Zusatznutzen aufweist. Daran ist auch die verbreiterte Marktexklusivität geknüpft, die das Handelsblatt ebenfalls anprangert.
„Slicing“ nicht zulässig
Ein weiterer Vorwurf lautet, dass die Firmen vor allem bei einer Krankheit aktiv seien, die keineswegs selten sei, aber das große Geld verspreche, nämlich bei Krebs. Das hänge offenbar auch damit zusammen, dass sich mittlerweile anhand von speziellen Untersuchungsmethoden eher häufige Krebsarten leicht unterteilen lassen, was auch als „Slicing" (in Scheiben schneiden) bezeichnet werde. Ein gutes Beispiel dafür sei die chronische lymphatische Leukämie, die häufigste Form des Blutkrebses. Auch diesen Vorwurf weist die forschende Pharmaindustrie vehement zurück. Die EU-Regelungen verböten ausdrücklich Untergruppen bezüglich des Orphan Drug-Status, und dies werde auch konsequent umgesetzt.
Nur wenige Blockbuster
Zudem kritisierte das Handelsblatt die Ausnutzung der zehnjährigen Marktexklusivität (EU), eine Zeit, in der die Hersteller nahezu ohne Korrektiv jeden Preis verlangen könnten. Für die GKV-Erstattung werde der Zusatznutzen mit der Zulassung des Medikaments einfach unterstellt. Der Gemeinsame Bundesausschuss dürfe lediglich dessen Umfang bestimmen. Auch hier hält der vfa dagegen. Da es für ein Orphan-Medikament nur wenige Anwender gebe, werde damit in der Regel kein großer Umsatz erzielt, auch wenn der Preis pro Packung bei einigen Orphan Drugs zu den höchsten im Arzneimittelwesen gehöre. Derzeit würden in Deutschland im ambulanten Bereich 68 Medikamente mit aktivem Orphan-Drug-Status verordnet. Auf diese entfielen 2015 nur 3,1 Prozent der GKV-Arzneimittelmittelausgaben (1,178 Milliarden Euro).
BPI: Zynische Kostendebatte
Auch der BPI betonte, dass Orphan Drugs im deutschen Erstattungssystem kein Selbstläufer seien. Der Anteil der Medikamente für seltene Erkrankungen am GKV-Arzneimittelbudget liege laut IMS Health-Studie bei gerade 3,5 Prozent, sagt Norbert Gerbsch, stellvertretender Hauptgeschäftsführer des BPI. Hier eine Kostendebatte zu entfachen und diese zudem mit Ängsten vor angeblich unsicheren Medikamenten zu schüren, sei geradezu zynisch den Betroffenen gegenüber.
Hier kommen Sie zum Plusminus-Beitrag Seltene Krankheiten als Geldquelle (abrufbar bis 5. Oktober 2017).























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.