
- DAZ.online
- News
- Pharmazie
- FDA lässt Gentherapie ...
Luxturna
FDA lässt Gentherapie gegen erblich bedingte Augenerkrankung zu
Stuttgart - 21.12.2017, 15:23 Uhr
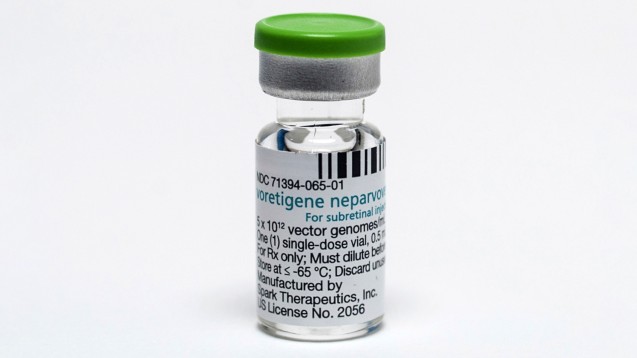
Die FDA hat eine Gentherapie gegen eine erbliche Form der Erblindung zugelassen. (Foto: picture alliance / AP Photo)
Wie lange hält der Effekt?
Sicherheit und Wirksamkeit wurden in einem klinischen Entwicklungsprogramm an 41 Patienten zwischen vier und 44 Jahren nachgewiesen. Zudem wurde eine Phase-III-Studie mit 31 Teilnehmern durchgeführt, in der über einen Zeitraum von einem Jahr die Fähigkeit der Probanden untersucht wurde, sich in einem Labyrinth bei verschiedenen Lichtverhältnissen zurechtzufinden. Im Gegensatz zur Kontrollgruppe verbesserten sich die Patienten, die die Therapie erhielten, hier signifikant. Die Behandlung hatte jedoch keine signifikanten Auswirkungen auf die Sehschärfe im Hellen. Insgesamt besserte sich die Lebensqualität der meisten Patienten spürbar, von einer vollständigen Heilung ist Luxturna aber weit entfernt.
Die häufigsten Nebenwirkungen waren gerötete Augen, Katarakt, erhöhter Augendruck und Netzhautrisse. Diese unerwünschten Wirkungen seien aber auf den Eingriff zurückzuführen, nicht auf die Therapie selbst, heißt es. Sie bildeten sich in den meisten Fällen vollständig zurück. Nebenwirkungen, die auf den Einsatz des AAV-Vektors zurückführen sind, oder unerwünschte Immunreaktionen wurden bislang nicht beschrieben.
Unklar ist bislang, wie lange die Wirkung anhält. Die zulassungsrelevanten Studien belegen einen Zeitraum von einem Jahr, denn so lange wurden die Teilnehmer beobachtet. Frühere, kleinere Studien deuten an, dass der Effekt mindestens drei Jahre lang anhält.
Kosten bis zu einer Million Dollar?
Die neue Zulassung bezeichnete FDA-Chef Scott Gottlieb als „Meilenstein“. „Gentherapie wird eine Stütze in der Behandlung und vielleicht auch der Heilung von vielen unserer schlimmsten und hartnäckigsten Krankheiten sein. Wir sind an einem Wendepunkt bei dieser neuen Therapieform." Über den Preis der neuen Therapie wird derzeit nur spekuliert. Es könnten aber Kosten bis zu einer Million Dollar für die Behandlung beider Augen entstehen. Gründe für den hohen Preis sind die lange Entwicklungszeit und die geringe Patientenzahl.
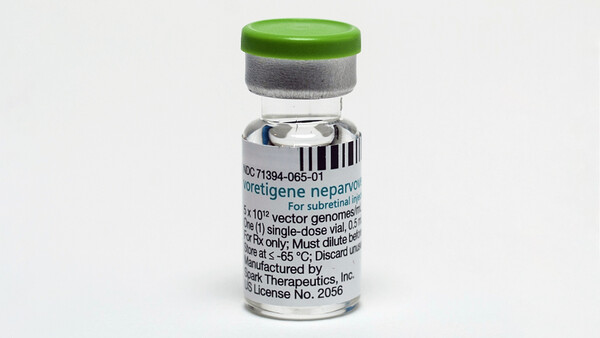
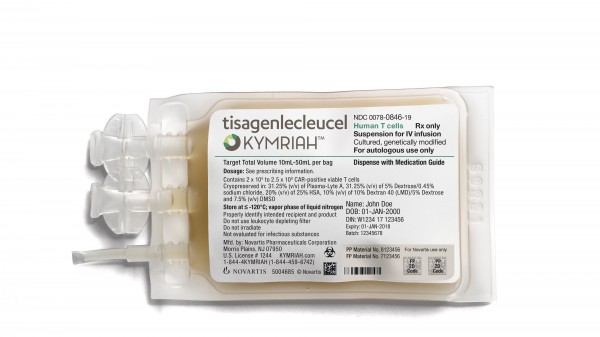
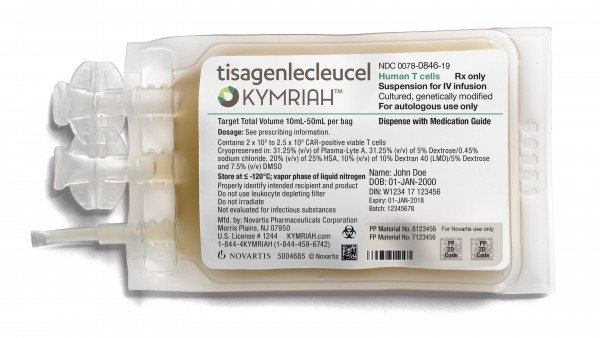
Luxturna ist nicht die erste in den USA zugelassene Gentherapie: Kymriah (Tisagenlecleucel) ist beispielsweise als der erste CAR-T-Zell-Therapie-Wirkstoff zur Behandlung einer bestimmten Form der akuten lymphatischen Leukämie (ALL) zugelassen, es war die erste Gentherapie in den USA überhaupt. Mit Yescarta wurde dann im Oktober die zweite CAR-T-Zell-Therapie von der US-Arzneimittelbehörde FDA zugelassen.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.