
- DAZ.online
- News
- Politik
- Neuordnung des ...
Anpassung an EU-Vorgaben
Neuordnung des Tierarzneimittelrechts im Eiltempo
Süsel - 01.02.2021, 12:15 Uhr

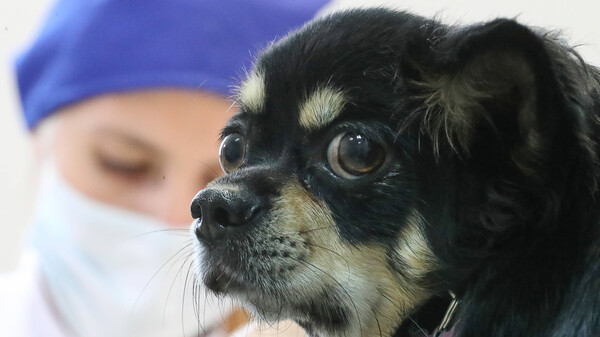
Entsprechend der Vorgabe der EU-Verordnung wird der Versand von Rx-Tierarzneimittel im Einzelhandel auch im geplanten TAMG verboten. (Foto: thodonal / stock.adobe.com)
Das Bundeslandwirtschaftsministerium hat den Entwurf für ein neues Tierarzneimittelgesetz vorgelegt. Alle Regelungen für Tierarzneimittel sollen aus dem Arzneimittelgesetz entfernt und in einer neuen Systematik unter Beachtung von EU-Vorgaben geregelt werden. Die Tierärzteorganisationen kritisieren die unerwartete Präsentation des Entwurfs und den knappen Zeitplan. Inhaltlich besteht offenbar großer Diskussionsbedarf.
Gemäß dem Referentenentwurf des Bundeslandwirtschaftsministeriums für ein neues Tierarzneimittelgesetz (TAMG) sollen alle Vorschriften für Tierarzneimittel aus dem Arzneimittelgesetz (AMG) entfernt und in ein eigenständiges Gesetz überführt werden. Hintergrund ist die Verordnung (EU) 2019/6 des Europäischen Parlaments und des Rates vom 11. Dezember 2018 über Tierarzneimittel, die am 28. Januar 2022 in Kraft treten wird und dann unmittelbar in allen EU-Ländern gilt. Um Diskrepanzen mit dem bisherigen Recht zu verhindern, muss bis dahin eine nationale Regelung vorliegen, die auf die EU-Verordnung eingeht und weitere nationale Vorschriften enthält.
Tierärzte kritisieren engen Zeitplan und intransparenten Prozess
Die maßgeblichen Tierärzteorganisationen erklärten am 26. Januar 2021, die Präsidenten der Bundestierärztekammer, des Bundesverbands der beamteten Tierärzte und des Bundesverbands Praktizierender Tierärzte (bpt) hätten Bundeslandwirtschaftsministerin Julia Klöckner (CDU) in der vorherigen Woche schriftlich aufgefordert, die Umsetzung des TAMG in dieser Legislaturperiode zu stoppen, „damit ein transparenter Diskussionsprozess möglich wird“. Die Verbände seien sich darin einig, „dass sie sich an einem derart intransparenten und unausgereiften Verfahren weder beteiligen können noch wollen“. In den beiden Jahren seit der Verabschiedung der EU-Verordnung habe kein fachlicher Austausch stattgefunden und nun sei „völlig unerwartet“ ein Gesetzentwurf mit einer Stellungnahmefrist von nur drei Wochen vorgelegt worden. Schon auf den ersten Blick hätten sich rechtlich-handwerkliche Fehler im Entwurf gezeigt, erklärte der bpt. Für einen transparenten Diskussionsprozess mit ausreichend Zeit stünden die Verbände jedoch zur Verfügung.
Alte Konzepte neu geordnet
Die Regelungen sollen im geplanten TAMG anders als bisher im AMG geordnet werden, teilweise werden neue Begriffe verwendet. Der TAMG-Entwurf greift vielfach auf die EU-Verordnung 2019/6 zurück und verweist auf die dortigen Regeln, aber er folgt nicht dem Aufbau der EU-Verordnung. Da das TAMG als eigenständiges Gesetz angelegt ist, sind darin auch alle grundlegenden Aspekte des Arzneimittelrechts enthalten, die bisher für alle Arzneimittel gemeinsam geregelt werden, beispielsweise Zulassung, Herstellung, Kennzeichnung, Fachinformation, Großhandel, Schutz vor Täuschung, Arzneibuch, Pharmakovigilanz, Überwachung und das Verbot bedenklicher Tierarzneimittel. Dabei werden teilweise neue Formulierungen gewählt. Da Tierarzneimittel zu einem eigenständigen Begriff werden, soll im Apothekengesetz klargestellt werden, dass sich der Sicherstellungsauftrag der Apotheken weiterhin auf alle Arzneimittel einschließlich Tierarzneimittel bezieht.
Rx-Versandverbot für Tierarzneimittel
Doch es geht nicht nur um neue Formulierungen in neu geordneten Paragrafen, sondern auch um inhaltliche Änderungen. Die Verschreibungspflicht für Tierarzneimittel soll sich nicht mehr an Stoffen, sondern an Arzneimitteln orientieren. Sie soll jeweils von der zuständigen Bundesoberbehörde anhand von Kriterien der EU-Verordnung festgelegt werden. Obwohl die EU-Verordnung keine Apothekenpflicht vorsieht, sollen Tierarzneimittel und veterinärmedizinische Produkte in Kategorien mit und ohne Apothekenpflicht eingeteilt werden. Zur Abgrenzung zwischen apothekenpflichtigen und frei verkäuflichen Tierarzneimitteln soll eine neue Verordnung erlassen werden. Außerdem sollen die administrativen Abläufe für den innergemeinschaftlichen Parallelhandel mit Tierarzneimitteln in einer neuen Verordnung geregelt werden.
Entsprechend der Vorgabe der EU-Verordnung wird der Versand von Rx-Tierarzneimitteln im Einzelhandel verboten. Von der Möglichkeit der EU-Verordnung, einen rein nationalen Versand zuzulassen, will der deutsche Gesetzgeber keinen Gebrauch machen. Für Rx-Tierarzneimittel soll damit künftig auf Veranlassung der EU vorgeschrieben werden, was für Rx-Humanarzneimittel als europarechtlich problematisch galt. Der Versand von nicht verschreibungspflichtigen Tierarzneimitteln soll unter Beachtung der EU-Verordnung in Deutschland zulässig sein.
Unklares zur Preisbindung und Rezeptur
Wie das AMG soll auch das TAMG eine Preisbindung enthalten, die einheitliche Apothekenabgabepreise sicherstellt. Nach dem vorgesehenen Wortlaut würde dies allerdings nicht nur verschreibungspflichtige, sondern alle apothekenpflichtigen Arzneimittel betreffen. Ob dies eine beabsichtigte Änderung oder ein redaktionelles Versehen ist, kann dem Referentenentwurf nicht entnommen werden. Weitere Fragen ergeben sich aus den Bestimmungen zur erlaubnisfreien Herstellung. Der Wortlaut des Entwurfs kann als Einschränkung der Rezepturherstellung von Tierarzneimitteln verstanden werden. Die zugrundeliegende EU-Verordnung lässt Rezepturen jedoch ausdrücklich zu. Eine genauere Betrachtung dieser und weiterer Aspekte des geplanten TAMG finden Sie in dieser Woche in der DAZ-Printausgabe 5/2021.
BAH sieht Anregung für Human-Arzneimittel
Außerdem bietet der TAMG-Entwurf Anregungen für Regelungen zu Human-Arzneimitteln. Der Bundesverband der Arzneimittel-Hersteller (BAH) hat in einer ersten Stellungnahme bereits Sympathie für die mittel- statt stoffbezogene Verschreibungspflicht geäußert. Dazu heißt es vom BAH: „Der BAH hat bereits seit Längerem eine Änderung des Switchverfahrens in Gestalt eines Verwaltungsverfahrens gefordert.“ Offenbar verspricht sich der BAH davon Vereinfachungen für den Switch von Rx- zu OTC-Arzneimitteln. Der BAH kündigt bis zum 8. Februar eine ausführliche Stellungnahme an.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.