13:08 Uhr
Biontech: Antrag auf Impfstoffzulassung für Kinder ab zwölf gestellt
Der deutsche Impfstoffhersteller Biontech und sein US-Partner Pfizer haben nach eigenen Angaben bei der europäischen Zulassungsbehörde EMA die Zulassung ihres Corona-Vakzins für Kinder und Jugendliche im Alter von 12 bis 15 Jahren beantragt. Dabei gehe es um die Anpassung und Erweiterung der bestehenden Zulassung auf diese Altersgruppe, teilten die Unternehmen am Freitag mit. Sobald die EMA die Änderung genehmige, werde die angepasste bedingte Zulassung in allen 27 Mitgliedsstaaten der EU gültig sein.
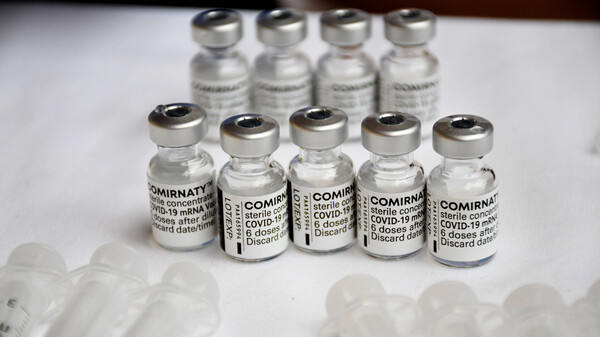
Comirnaty® ist in der EU und in den USA bislang erst für Menschen ab 16 Jahren bedingt zugelassen. In den USA wurde bei der Arzneimittelbehörde FDA bereits der Antrag auf die Erweiterung der bestehenden Notfallzulassung für den Impfstoff auf die Gruppe der 12- bis 15-Jährigen eingereicht.
Biontech und Pfizer hatten kürzlich mitgeteilt, dass eine klinische Studie in der Altersgruppe von 12 bis 15 Jahren in den USA eine Wirksamkeit von 100 Prozent gezeigt habe. Die Impfung sei gut vertragen worden. Die Nebenwirkungen hätten jenen in der Altersgruppe von 16 bis 25 Jahren entsprochen, erklärten die Unternehmen.
Für die Prüfung von Zulassungsanträgen für Corona-Impfstoffe braucht die EMA in der Regel wenige Wochen. Das heißt, dass die EU-Zulassung im günstigen Fall bei einer Bearbeitungsdauer von vier bis sechs Wochen Anfang bis Mitte Juni erfolgen könnte. Anschließend könnte es mit den Impfungen der 12- bis 15-Jährigen losgehen, sofern ausreichend Impfstoff zur Verfügung steht. Mit Blick auf das kommende Schuljahr und die angestrebte Erweiterung der geimpften Bevölkerungsgruppen mit dem Ziel einer Herdenimmunität wäre dies ein wichtiger Schritt.
Parallel dazu läuft die klinische Studie von Biontech und Pfizer zur Wirkung und Sicherheit von Comirnaty® bei Kindern zwischen sechs Monaten bis einschließlich elf Jahren weiter. Biontech geht nach eigenen Angaben davon aus, dass belastbare Daten daraus bis September verfügbar sein werden. Bis die ersten Kinder aus dieser Altersgruppe mit dem Vakzin geimpft werden können, wird es folglich noch dauern, da Biontech/Pfizer erst nach diesem Zwischenschritt einen Zulassungsantrag bei der EMA stellen werden. Dessen Prüfung wird dann voraussichtlich erneut wenige Woche dauern.
12:44 Uhr
Zeitpunkt für mehr Rechte von Geimpften noch unklar
Wann die meisten Corona-Einschränkungen für vollständig Geimpfte und Genesene fallen, ist noch unklar. Die Regierung wolle eine entsprechende Verordnung aber „mit großem Druck und großem zeitlichem Ehrgeiz“ angehen, sagte Regierungssprecher Steffen Seibert am Freitag in Berlin.
Bundesjustizministerin Christine Lambrecht (SPD) hatte am Donnerstag einen Vorschlag für eine Verordnung dazu gemacht. Insbesondere von Beschränkungen für private Treffen und nächtlichen Ausgang sollen diese Gruppen ausgenommen werden.
Wie rasch die neue Verordnung dann im Kabinett und danach in Bundestag und Bundesrat verabschiedet werden kann, ist aber noch offen. Dies hänge von den anderen Beteiligten im Parlament und den Ländern ab, sagte Seibert. „Die Bundesregierung möchte mit dieser Verordnung schnell in Bundestag und Bundesrat gehen.“
Zunächst solle Lambrechts Vorschlag nun zwischen den Ministerien abgestimmt werden, erklärte Seibert. „Anfang der Woche wollen wir als Bundesregierung damit fertig sein.“ Über mögliche Änderungen will die Bundesregierung sich mit Bundestag und Ländern schon vor dem Kabinettsbeschluss einig werden, weil spätere Änderungen das Verfahren noch einmal deutlich verlängern würden.
Man sei in einer „Zwischenphase“, sagte Seibert. Einerseits hätten bereits Millionen Bürger in Deutschland einen vollständigen Impfschutz, gleichzeitig gebe es noch deutlich mehr, die ihn nicht haben. Es gehe um eine komplexe Aufgabe und um „Grundrechte, die geachtet und geschützt werden müssen“.
Die Bundesregierung könne Ausnahmen von den Corona-Beschränkungen erst jetzt regeln, weil die in der vergangenen Woche in Kraft getretene Bundes-Notbremse die Möglichkeit zu einer solchen Verordnung erst geschaffen habe, erläuterte ein Sprecher des Bundesjustizministeriums.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.