
- DAZ.online
- News
- Pharmazie
- Johnson & Johnson-...
ENSEMBLE-Studie
Johnson & Johnson-Impfstoff: Auch gegen die neuen Varianten wirksam
Remagen - 28.04.2021, 07:00 Uhr
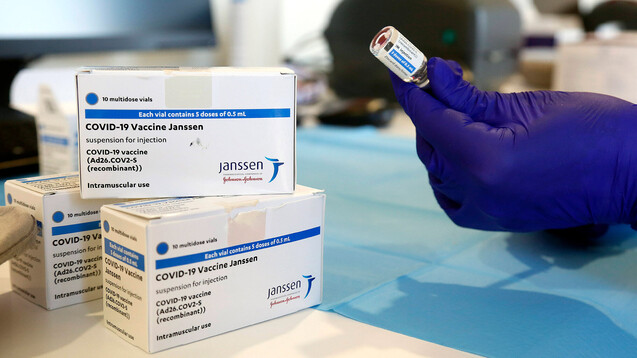
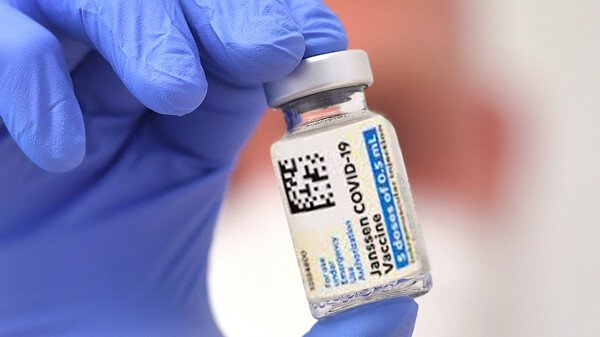
Der COVID-19- Impfstoff von Janssen (Johnson & Johnson) schützte in den Studien auch zuverlässig vor schwerem COVID-19 durch SARS-CoV-2-Varianten. (s / Foto: IMAGO / Insidefoto)
Vor wenigen Tagen wurden im „New England Journal of Medicine“ die Ergebnisse der Primäranalyse der zulassungsrelevanten Phase 3-Studie ENSEMBLE veröffentlicht. Hiernach erwies sich die COVID-19 Vaccine Janssen bereits sieben Tage nach der Impfung als wirksam gegen schweres/kritisches COVID-19. Außerdem verhindert sie offenbar auch symptomatische Infektionen mit den Varianten, die in Südafrika und Brasilien vorherrschen.
Der COVID-19-Impfstoff von Johnson & Johnson, der nur einmal verabreicht werden muss, hat in der Phase-3-Studie ENSEMBLE alle primären und wichtigsten sekundären Endpunkte erreicht. Dies geht aus der Veröffentlichung der Primäranalyse durch die Studiengruppe im „New England Journal of Medicine“ hervor.
Die Topline-Ergebnisse der Studie waren bereits im Januar bekannt gemacht worden. Die „COVID-19 Vaccine Janssen“ (Ad26.COV2.S), die von Johnson & Johnsons Pharmasparte Janssen entwickelt wurde, besteht aus einem rekombinanten, nicht vermehrungsfähigen humanen Adenovirus Typ26-basierten Vektor, der die DNA für ein SARS-CoV-2 Spike-Protein in voller Länge in einer präsfusionsstabilisierten Konformation trägt.
Acht Länder auf drei Kontinenten
Die multinationale, randomisierte, doppelblinde, Placebo-kontrollierte Phase-3-Studie ENSEMBLE (NCT04505722) begann am 21. September 2020. Der Datenstichtag für die vorliegende Analyse war der 22. Januar 2021. Insgesamt wurden 44.325 erwachsene Teilnehmer im Verhältnis 1:1 nach dem Zufallsprinzip einer Einzeldosis Ad26.COV2.S (5×1010 Viruspartikel) oder Placebo zugeordnet. 34 Prozent der Teilnehmer waren über 60 Jahre alt.
Die Studie wurde in acht Ländern auf drei Kontinenten durchgeführt: 44 Prozent der Teilnehmer entfielen auf die USA, 41 Prozent auf Mittel- und Südamerika (Argentinien, Brasilien, Chile, Kolumbien, Mexiko, Peru) und 15 Prozent auf Südafrika. 41 Prozent der teilnehmenden Personen hatten Komorbiditäten, die mit einem erhöhten Risiko für das Fortschreiten für schweres/kritisches COVID-19 verbunden sind, darunter Fettleibigkeit (28 Prozent), Bluthochdruck (10 Prozent), Typ-2-Diabetes (7 Prozent) und oder HIV (3 Prozent).
Die primären Endpunkte waren die Wirksamkeit der Impfung gegen mittelschweres bis schweres/kritisches COVID-19 mit Beginn mindestens 14 Tage (≥ 14 Tage) bzw. mindestens 28 Tage (≥ 28 Tage) nach der Impfung. Die Per-Protokoll-Population, die für die Wirksamkeitsanalyse herangezogen wurde, umfasste 39.321 SARS-CoV-2–negative Teilnehmer, die fast zu gleichen Teilen den Impfstoff oder Placebo erhalten hatten.
Schweres/kritisches COVID-19 zu 85 Prozent verhindert
Die ENSEMBLE-Daten weisen gegen mittelschweres bis schweres/kritisches COVID-19 ≥ 14 Tage nach der Impfung eine Wirksamkeit von 67 Prozent aus und ≥ 28 Tage nach der Impfung von 66 Prozent. Schweres/kritisches COVID-19 kann die Vakzine nach der Studie noch deutlich besser verhindern. Hierfür wurde ≥ 14 Tage nach der Impfung eine Wirksamkeit von 77 Prozent ermittelt und ≥ 28 Tage nach der Impfung etwas über 85 Prozent. Der Schutz war im Allgemeinen über Ethnien und Altersgruppen, einschließlich Erwachsener über 60 Jahre, und Personen mit und ohne Komorbiditäten konsistent.
Der Beginn der Wirksamkeit war hinsichtlich der Verhinderung einer schweren/kritischen Erkrankung schon sieben Tage nach der Impfung und bezüglich mittelschwerer bis schwerer/kritischer Erkrankung 14 Tage danach erkennbar. Außerdem nahm die Wirksamkeit über ungefähr acht Wochen nach der Impfung weiter zu.
Nach ergänzenden Daten, die seit der Bekanntgabe der Topline-Results im Januar gesammelt wurden, gibt es keine Hinweise darauf, dass der Schutz im Laufe der Zeit abnimmt. Hierfür waren ungefähr 3.000 Teilnehmer 11 Wochen lang und 1.000 Teilnehmer 15 Wochen lang nachbeobachtet worden.
Nebenwirkungen leicht bis mittelschwer und vorübergehend
Die Sicherheits-Subpopulation umfasste 3.356 Teilnehmer in der Impfstoffgruppe und 3.380 in der Placebo-Gruppe. Insgesamt war die Reaktogenität mit dem COVID-19-Impfstoff höher als mit Placebo, aber die Reaktionen waren im Allgemeinen leicht bis mittelschwer und vorübergehend. In der Impfstoffgruppe wurden als häufigste Nebenwirkungen Schmerzen an der Injektionsstelle (49 Prozent der Teilnehmer), Kopfschmerzen (39 Prozent), Müdigkeit (33 Prozent), Myalgie (33 Prozent) und Übelkeit (14 Prozent) beobachtet. Außerdem wurden in der Impfstoffgruppe elf venöse thromboembolische Ereignisse registriert, gegenüber drei in der Placebo-Gruppe. Die meisten der betroffenen Teilnehmer hatten zugrunde liegende Erkrankungen und prädisponierende Faktoren, die zu diesen Ereignissen beigetragen haben könnten.
Wirksamkeit gegen die neuen Variants of Concern
In den USA wurde nach Genomsequenzierungen vorwiegend die Referenzsequenz (Wuhan-Hu-1 einschließlich der D614G-Mutation) gefunden (96 Prozent), in Südafrika überwiegend die 20H/501Y. V2-Variante (B.1.351) (94 Prozent), während in Brasilien zu 31 Prozent die Referenzsequenz detektiert wurde und zu 69 Prozent die Referenzsequenz mit der E484K Mutation (P.2-Linie).
Trotz der hohen Prävalenz der Variante B.1.351 in Südafrika war die Wirksamkeit der Impfung dort kaum beeinträchtigt. ≥ 14 Tage nach der Verabreichung lag sie für die Verhinderung mittelschwerer bis schwerer/kritische Erkrankungen bei 52 Prozent und für schweres/kritisches COVID-19 bei 73 Prozent. ≥ 28 Tage nach der Verabreichung wurden Wirksamkeiten von 64 bzw. 82 Prozent ermittelt. Die Wirksamkeit wurde auch bei Teilnehmern in Brasilien beibehalten, mit einer Wirksamkeit von 68 Prozent gegen mittelschwere bis schwere/kritische Erkrankungen und 88 Prozent gegen schwere/kritische Erkrankungen ≥ 28 Tage nach der Verabreichung.
Nutzen-Risiko-Profil weiterhin positiv
Die COVID-19 Vakzine Janssen ist in der EU seit dem 11. März 2021 bedingt zugelassen. Nach der Überprüfung von Sicherheitsbedenken wegen erhöhter Thromboserisiken bestätigte das Pharmacovigilance Risk Assessment Committee (PRAC) der Europäischen Arzneimittel-Agentur (EMA) am 20. April 2021, dass das Nutzen-Risiko-Profil insgesamt weiterhin positiv ist. Auch in den USA wurden die zwischenzeitlich pausierten Impfungen mit der Johnson & Johnson-Vakzine vor wenigen Tagen wieder aufgenommen.
Wann kommt der Impfstoff und wie viel kommt?
Die EU-Kommission hat bisher Impfdosen für 200 Millionen Menschen bestellt. 36,7 Millionen sollen davon nach Deutschland gehen. Nach aktuellen Informationen des Redaktionsnetzwerks Deutschland (RND) soll Johnson & Johnson für das zweite Quartal eine Lieferzusage von zehn Millionen Dosen gemacht haben. Allerdings soll eine bevorstehende Lieferung nach Deutschland voraussichtlich einen geringeren Umfang haben als ursprünglich erwartet. Auch hier scheint also wieder mal nicht alles glatt zu gehen. Wie auch immer: „Die Impfdosen werden ab Mai in den Arztpraxen verimpft werden“, zitiert das RND einen BMG-Sprecher.






















5 Kommentare
Erste janssen impfunh
von Ludwig rickauet am 26.05.2021 um 15:37 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Covid 19 Vakzine Janssen
von Michael Nell am 25.05.2021 um 8:27 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Formulierungen : Der Schutz war im Allgemeinen über Rassen und Altersgruppen, einschließlich Erwachsener über 60 Jahre, und Personen mit und ohne Komorbiditäten konsistent.
von Straube am 07.05.2021 um 12:44 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Formulierungen : Der Schutz war im
von DAZ.online am 07.05.2021 um 13:06 Uhr
AW: Formulierungen : Der Schutz war im
von Frank Schellinger am 10.05.2021 um 20:54 Uhr
Das Kommentieren ist aktuell nicht möglich.