
- DAZ.online
- News
- Pharmazie
- Remdesivir kurz vor ...
COVID-19
Remdesivir kurz vor Zulassung in der EU
Stuttgart - 19.05.2020, 10:15 Uhr
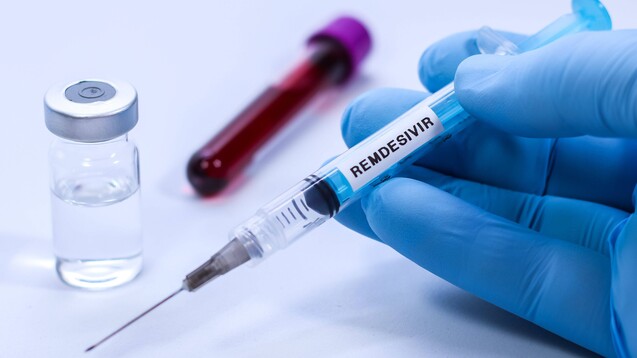
Nachdem die USA und Japan bereits bei der Zulassung von Remdesivir bei COVID-19 vorangegangen sind, plant auch die EMA, das erste Corona-Arzneimittel in den kommenden Tagen zu genehmigen. ( r / Foto: imago images / Fotoarena)
Erst in der vergangenen Woche sorgte die EMA dafür, dass das Virostatikum Remdesivir auch in der EU zur Behandlung von Patienten mit COVID-19 breiter eingesetzt werden darf, nachdem die USA und Japan das Gilead-Arzneimittel bereits per Ausnahmegenehmigung zugelassen hatten. Nun kündigt die EMA an, dass Remdesivir kurz vor einer bedingten Marktzulassung steht.
Die Europäische Arzneimittel-Agentur (EMA) plant kurzfristig die bedingte Marktzulassung von Remdesivir für die Behandlung von COVID-19-Patienten. Dies erklärte der Direktor der Europäische Arzneimittel-Agentur, Guido Rasi, auf eine Frage des gesundheitspolitischen Sprechers der größten Fraktion im Europäischen Parlament, Dr. med. Peter Liese (EVP, Christdemokraten), bei einer Anhörung im Ausschuss für Umwelt und Gesundheit des Europäischen Parlamentes. Erst in der vergangenen Woche hatte die EMA einen breiteren Einsatz des RNA-Polymerase-Inhibitors angestoßen.
Mehr zum Thema
EMA erweitert Einsatz von Remdesivir
Compassionate Use: Mehr Coronapatienten erhalten Remdesivir
Nach Notfallzulassung in den USA
EMA prüft Remdesivir
Beschleunigte Zulassung bei der FDA?
Widersprüchliches zu Remdesivir – hilft es bei COVID-19?
Zuvor war Remdesivir in der EU nur im Rahmen von Härtefallprogrammen (Compassionate Use) eingesetzt worden, und zwar ausschließlich bei COVID-19-Patienten, die eine invasive maschinelle Beatmung benötigen. Am 11. Mai riet die EMA, diesen Compassionate Use zu erweitern, damit mehr COVID-19-Erkrankte Remdesivir erhalten können. Seither dürfen zusätzlich zu Patienten, die sich einer invasiven maschinellen Beatmung unterziehen, auch hospitalisierte Patienten Remdesivir erhalten, wenn sie zusätzlichen Sauerstoff benötigen, bei nicht-invasiver Beatmung per High-Flow-Sauerstofftherapie oder mit ECMO (extrakorporale Membranoxygenierung). In den USA und Japan ist Remdesivir bereits per Notfallgenehmigung verfügbar. Diese Ausnahmegenehmigung rückt nun auch in Europa in greifbare Nähe.
Remdesivir: „wahrscheinlich wirksam und nebenwirkungsarm"
Der Ausschuss für Humanarzneimittel (CHMP) der EMA prüft Remdesivir bereits in einem Rolling Review, einer fortlaufenden Überprüfung. Das Rolling-Review-Verfahren ist ein Regulierungsinstrument, das die EMA nutzen kann, um ein vielversprechendes Arzneimittel während eines Notfalls im Bereich der öffentlichen Gesundheit, wie beispielsweise der laufenden Pandemie, zu bewerten und eine bedingte Marktzulassung zu erteilen.
Bedingte Marktzulassung
Eine bedingte Marktzulassung bedeutet, dass das Arzneimittel nach Einschätzung der Experten wahrscheinlich wirksam und nebenwirkungsarm ist, dass man aber im Rahmen der Behandlung weiterhin genau untersuchen muss, ob diese Annahme stimmt. Peter Liese erklärt hierzu: „Ich halte die bedingte Marktzulassung von Remdesivir für richtig. Es ist eine gute Nachricht für viele Patienten, die schwer an COVID-19 erkrankt sind und um ihr Leben fürchten.“
Die bisherigen Untersuchungen hätten offensichtlich gezeigt, dass Remdesivir den Krankheitsverlauf abmildert, vielleicht sogar die Todesrate absenken kann und dass die Nebenwirkungen vertretbar sind, so der Arzt Liese weiter. Diese Begründung lieferte auch die FDA im Rahmen der dortigen Remdesivir-Genehmigung. Grundlage für diese Einschätzung bildet eine Zwischenauswertung der NIAID-ACTT-Studie aus den Vereinigten Staaten. Remdesivir verkürzte dort die Krankheitsdauer und lieferte Hinweise auf eine Mortalitätssenkung. Eine chinesische Untersuchung hingegen fand keine Vorteile durch eine Remdesivirbehandlung.
Genehmigung Voraussetzung für Erstattung der Krankenkassen
Liese weiter: „Wir müssen allerdings weiter genau beobachten und die Daten fortwährend analysieren. Wichtig ist, dass das Medikament nun in ausreichender Zahl zur Verfügung steht.“ Auch hier unterstützen neue Daten, denen zufolge eine fünftägige Remdesivirbehandlung einer zehntägigen nicht unterlegen ist. Gilead habe Peter Liese zudem „persönlich versichert“, dass sie Remdesivir europäischen Patienten zur Verfügung stellt, wenn die bedingte Marktzulassung erfolgt sei. Die bedingte Marktzulassung sei auch eine Voraussetzung, damit zu mindestens in Deutschland die Krankenkassen die Kosten übernähmen, schließt Liese.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.