
- DAZ.online
- News
- Pharmazie
- EMA prüft Remdesivir
Nach Notfallzulassung in den USA
EMA prüft Remdesivir
Stuttgart - 04.05.2020, 17:50 Uhr
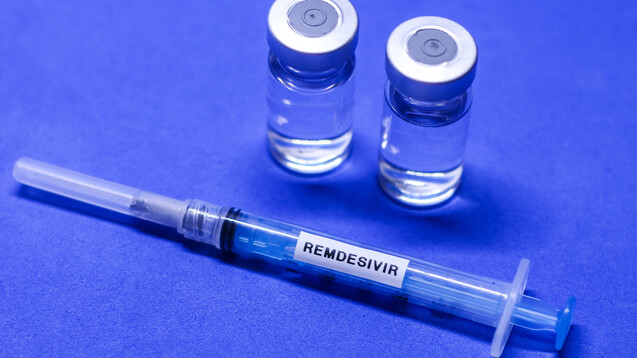
Am 1. Mai 2020 ließ die FDA das Virostatikum Remdesivir bei COVID-19 im Rahmen einer Notfallgenehmigung (Emergency Use Authorization, EUA) zu. Auch die EMA prüft Remdesivir bei SARS-CoV-2. (ch/Foto: imago images / Fotoarena)
Remdesivir ist zugelassen – bislang nur durch die FDA in den Vereinigten Staaten und nur in Form einer Notfallgenehmigung, die keiner formellen Zulassung entspricht. Das Virostatikum soll laut einer Studie in den USA die Krankheitsdauer bei COVID-19 verkürzen, es darf nur bei schwerem SARS-CoV-2-Infektionsverlauf eingesetzt werden, dann aber sowohl bei Erwachsenen als auch bei Kindern. Die EMA prüft Remdesivir ebenfalls.
Die FDA hat am 1. Mai 2020 Remdesivir die Notfallgenehmigung erteilt. Das Virostatikum darf in den Vereinigen Staaten künftig bei Erwachsenen und Kindern zur Behandlung von vermutetem oder laborbestätigtem COVID-19 eingesetzt werden, wenn diese mit einer schweren Erkrankung – definiert als SpO2 ≤ 94 Prozent (an Raumluft) und zusätzlichem Sauerstoffbedarf, erforderlicher mechanischer Beatmung oder extrakorporaler Membranoxygenierung (ECMO) – ins Krankenhaus eingeliefert werden. Die Anwendung von Remdesivir ist folglich auf ein stationäres Setting begrenzt. Die USA sind das erste Land, das nun – wenn auch nur per Ausnahmegenehmigung (Emergency Use Authorization, EUA) – ein gegen COVID-19 zugelassenes Arzneimittel hat.
Mehr zu Remdesivir bei COVID-19
Beschleunigte Zulassung bei der FDA?
Widersprüchliches zu Remdesivir – hilft es bei COVID-19?

Remdesivir bei Covid-19
Arzneimittel gegen das Coronavirus SARS-CoV-2: Studien starten
Die Genehmigung für den Einsatz von Remdesivir in Notfällen entspricht keiner gewöhnlichen Zulassung, das wäre ein deutlich aufwendigerer Prozess gewesen. Zurzeit gibt es nur wenige klinische Daten zu Remdesivir bei COVID-19 beim Menschen, nicht alle Untersuchungen haben einen Nutzen des Virostatikums bestätigt.
COVID-19 lebensbedrohlich und ohne zugelassene Therapie
In einem Brief an den Hersteller Gilead erklärt Denise M. Hinton, Chief Scientist bei der FDA, das rasche Inverkehrbringen von Remdesivir sei möglich, da SARS-CoV-2 eine ernste oder lebensbedrohliche Erkrankung hervorrufen könne. Es sei die Annahme vertretbar, dass Remdesivir wirksam bei COVID-19 ist und der mögliche Nutzen die potenziellen Risiken überwiegt, auch weil es keine zugelassene und verfügbare Alternative zu Remdesivir gibt.
Rolling Review für Remdesivir
Auch die Europäische Arzneimittel-Agentur EMA prüft das Virostatikum: Der Ausschuss für Humanarzneimittel (CHMP) der EMA hat ein Rolling Review, eine gleitende Überprüfung, von Remdesivir zur Behandlung von COVID-19 eingeleitet. Das Rolling-Review-Verfahren ist ein Regulierungsinstrument, das die EMA nutzen kann, um ein vielversprechendes Arzneimittel während eines Notfalls im Bereich der öffentlichen Gesundheit, wie beispielsweise der laufenden Pandemie, zu bewerten. Normalerweise müssen alle zulassungsrelevanten Arzneimitteldaten zu Beginn des Evaluationsverfahrens eingereicht werden. Im Falle einer gleitenden Überprüfung werden die CHMP-Berichterstatter ernannt, während die Entwicklung noch im Gange ist, und die Agentur überprüft die Daten, sobald sie verfügbar sind.
ACTT-Studie: Remdesivir verkürzte Krankheitsdauer
„Der Beginn der fortlaufenden Überprüfung von Remdesivir bedeutet lediglich, dass die Bewertung von Remdesivir begonnen hat und nicht, dass die Vorteile die Risiken überwiegen“, betont die EMA. Die Entscheidung des CHMP vom 30. April 2020, Remdesivir in einem Rolling Review fortlaufend zu prüfen, basiert der EMA zufolge auf vorläufigen Ergebnissen der ACTT-Studie (Adaptive COVID-19 Treatment Trial), der ersten klinischen Studie in den Vereinigten Staaten zu Remdesivir. Durchgeführt und gesponsert wird ACTT vom National Institute of Allergy and Infectious Diseases (NIAID), das Teil des Nationalen Gesundheitsinstituts NIH (National Institute of Health) ist. Die ACTT Studie war auch Grundlage der Notfallgenehmigung bei der FDA. Laut ACTT zeigten Patienten, die Remdesivir erhielten, eine 31 Prozent kürzere Genesungszeit als Patienten unter Placebo: Im Median waren Remdesivir-Patienten nach elf Tagen, Placebo-Patienten nach 15 Tagen genesen. Die Ergebnisse deuteten dem NIH zufolge auch auf einen Überlebensvorteil hin: Die Mortalitätsrate in der Remdesivir-Gruppe lag bei 8 Prozent, in der Placebogruppe bei 11,6 Prozent.
Wann kommt Remdesivir in der EU?
Die Ergebnisse der ACTT-Studie sind zum aktuellen Zeitpunkt nicht ausgewertet, es sei somit zu früh, um Schlussfolgerungen hinsichtlich des Nutzen-Risiko-Verhältnisses des Medikaments bei Patienten mit COVID-19 zu ziehen. Der CHMP will alle neuen Daten, die während des Remdesivir-Reviews verfügbar werden, in seine Bewertung einfließen lassen, einschließlich einer vor kurzem im Fachjournal Lancet veröffentlichten Studie aus China. Entgegen der ACTT-Zwischenanalyse aus den Vereinigten Staaten, verkürzte Remdesivir in der chinesischen Untersuchung weder die Krankheitsdauer, noch senkte es die Mortalität.
Obwohl der Gesamtzeitplan für die Überprüfung von Remedesivir zum jetzigen Zeitpunkt nicht vorhersehbar ist, erwartet der CHMP, dass das Rolling-Review-Verfahren es der EMA ermöglichen wird, ihre Bewertung im Vergleich zu einem regulären Zulassungsverfahren deutlich früher abzuschließen und dennoch gleichzeitig sicherzustellen, dass ein fundiertes wissenschaftliches Gutachten erstellt wird.
Remdesivir als Compassionate Use in der EU
Obwohl Remedesivir in der Europäischen Union noch nicht zugelassen ist, ist es für Patienten dennoch über klinische Studien und sogenannte Compassionate-Use-Programme, über die Patienten Zugang zu nicht zugelassene Arzneimittel in Notfallsituationen erhalten, verfügbar. Auch in Deutschland wird Remdesivir in Härtefallprogrammen untersucht.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.