
- DAZ.online
- News
- Pharmazie
- Arzneimittel gegen das ...
Remdesivir bei Covid-19
Arzneimittel gegen das Coronavirus SARS-CoV-2: Studien starten
Stuttgart - 02.03.2020, 09:00 Uhr

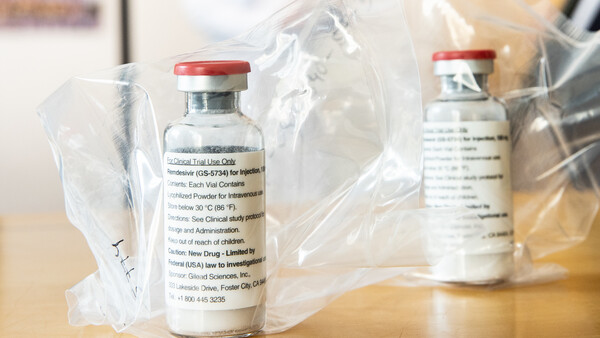
Remdesivir gilt als vielversprechender Kandidat zur Behandlung von SARS-CoV-2-bedingten COVID-19-Erkrankungen. Ursprünglich zur Behandlung von Ebola entwickelt, könnte Remdesivir (Gilead) auch bei Coronaviren wirken. (s / Foto: tilialucida / stock.adobe.com)
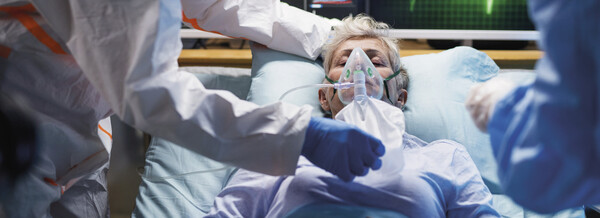
Remdesivir wird an COVID-19-Erkrankten untersucht
Bereits im Februar hat die erste klinische Studie in den USA zu Gileads Remdesivir an COVID-19-Erkrankten am University of Nebraska Medical Center (UNMC) in Nebraska begonnen. Das National Institute of Allergy and Infectious Diseases (NIAID) – Teil des National Institutes of Health (NIH), den Nationalen Gesundheitsinstituten – untersucht derzeit die Sicherheit und Wirksamkeit von Remdesivir an hospitalisierten Erwachsenen, die an COVID-19 erkrankt sind. Einer der Studien-Probanden war Passagier auf dem von SARS-CoV-2 betroffenen Kreuzfahrtschiff Diamond Princess.
Der Direktor des NIAID und Mitglied der U.S. Coronavirus Task Force, Anthony S. Fauci, M.D., erklärt:
Wir brauchen dringend eine sichere und wirksame Behandlung für COVID-19. Obwohl Remdesivir einigen Patienten mit COVID-19 verabreicht wurde, liegen uns keine soliden Daten vor, die darauf hinweisen, dass es das klinische Outcome der Patienten verbessern kann."
Anthony S. Fauci, M.D (Direktor des NIAID)
Das soll die randomisierte, doppelblinde und placebokontrollierte Studie nun ändern. Eingeschlossen werden Patienten, die labordiagnostisch SARS-CoV-2 bestätigt sind, wenn diese eine Lungenbeteiligung zeigen (Rasselgeräusche beim Atmen und zusätzliche Sauerstoffversorgung oder auffälliger Röntgenbefund oder künstliche Beatmung). COVID-19-Patienten mit nur milden Erkältungssymptomen dürfen an der Studie nicht teilnehmen.
Wirkt Remdesivir besser als Placebo?
Im Rahmen der Studie erhalten die SARS-CoV2-Infizierten für die Dauer ihres Klinikaufenthaltes (maximal jedoch zehn Tage) entweder initial 200 mg Remdesivir i.v. an Tag 1, gefolgt von täglich 100 mg Remdesivir i.v., oder ausschließlich Placebo. Die Studienärzte erheben fortlaufend Temperatur, Blutdruck und den zusätzlichen Sauerstoffbedarf, zudem sollen alle zwei Tage Blutproben, Nasen- und Rachenabstriche auf SARS-CoV-2 untersucht werden. Erste Ergebnisse der Remdesivir- und Placebogruppe sollen an Tag 15 verglichen werden, um festzustellen, ob Remdesivir den klinischen Nutzen stärker erhöht als Placebo. Laut NIH werden die Ergebnisse auf einer Sieben-Punkte-Skala bewertet, diese reicht von „vollständiger Genesung“ bis zum „Tod“.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.