
- DAZ.online
- News
- Pharmazie
- Metformin: FDA findet ...
Erster Engpass in Deutschland
Metformin: FDA findet NDMA nur in Fertigarzneimitteln, nicht im Wirkstoff
Stuttgart - 05.02.2020, 10:15 Uhr
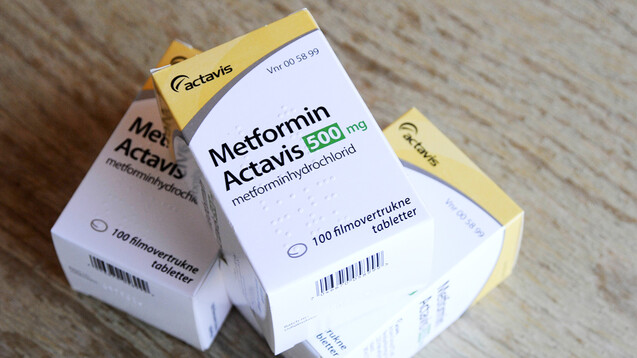
In den USA wurden bislang nur in Metformin von Actavis geringe NDMA-Mengen gefunden. Hier ist ein dänisches Präparat abgebildet. (s / Foto: imago images / Dean Pictures)
Die US-amerikanische Arzneimittelbehörde FDA hat am vergangenen Montag ihre Labor-Ergebnisse zur Prüfung von Metformin auf NDMA veröffentlicht. Spuren der Nitrosamin-Verunreinigung waren zuvor in einer geringen Anzahl von metforminhaltigen Arzneimitteln im Dezember 2019 außerhalb der EU gefunden worden. Die europäische Arzneimittelbehörde EMA hat sich bislang nicht detailliert zu dem Fall geäußert. In den USA liegen nun aber erste Messergebnisse öffentlich vor. Was bedeutet das für Deutschland?
Im Sommer 2018 begann mit dem Valsartan-Skandal die bis heute andauernde Nitrosamin-Krise. Seit September 2019 müssen pharmazeutische Unternehmen alle ihre chemischen Wirkstoffe auf Nitrosamine prüfen. Das war bislang nur eine Aufforderung der europäischen Arzneimittelbehörde EMA und wird sich wohl bald auch im Europäischen Arzneibuch (Ph. Eur.) rechtlich bindend wiederfinden.
Mehr zum Thema

Neue Arzneibuch-Monographie
Nitrosamin-Kontrollen für alle Stoffe kommen ins Europäische Arzneibuch

Kommentierende Analyse
Valsartan, Ranitidin, Metformin – und jetzt?

NDMA in Arzneimitteln
Metformin-Rückruf in der Schweiz
Konkret und öffentlichkeitswirksam ist mit Metformin zuletzt im Dezember 2019 ein Wirkstoff unter Verdacht geraten, der in der Diabetes-Therapie einen kaum zu ersetzenden Stellenwert hat. Bislang kam es nur in Singapur (drei Metformin-Präparate) und in der Schweiz aufgrund einer Verunreinigung mit NDMA lokal zu Rückrufen. Das BfArM (Bundesinstitut für Arzneimittel und Medizinprodukte) betonte bereits im vergangenen Dezember, dass nur „Spuren einer Verunreinigung, N-Nitrosodimethylamin (NDMA)“ in einer „geringen Anzahl von metforminhaltigen Arzneimitteln außerhalb der Europäischen Union (EU) gefunden“ wurden. Es sollen keine Daten vorliegen, die darauf hindeuten, dass Arzneimittel, die sich in der EU auf dem Markt befinden, betroffen sind, hieß es. Und die europäischen Überwachungsbehörden scheinen bis heute gemeinsam mit den pharmazeutischen Unternehmen daran zu arbeiten, entsprechende Arzneimittel, die sich auf dem europäischen Markt befinden, zu testen – denn bislang gab es dazu kein offizielles Update.
USA: Nur geringe NDMA-Mengen in Metformin von Actavis gefunden
Anders sieht es in den USA aus. Die US-amerikanische Arzneimittelbehörde FDA hat am vergangenen Montag erste Labor-Ergebnisse zur Prüfung von Metformin auf NDMA veröffentlicht. Daraus geht hervor, dass bislang nur in Metformin von Actavis NDMA gefunden wurde – in Mengen zwischen 0,01 und 0,02 µg. Damit liegt die Menge unter der tolerierten täglichen Aufnahmegrenze von 0,096µg. Bis jetzt hat die FDA somit keine Rückrufaktion für die USA empfohlen, doch die Untersuchungen sind auch dort noch nicht abgeschlossen.
Mehr zum Thema

In Asien entdeckte Verunreinigungen sind keine Überraschung – erste Rückrufe in der Schweiz
Nitrosamine in Metformin

US-Online-Apotheke Valisure
„Ranitidin bildet tausende von Nanogramm NDMA im Magen“

NDMA entsteht bei Wärme
Sollte Ranitidin besser in den Kühlschrank?
Die FDA erwähnt zudem, dass bislang nur in Fertigarzneimitteln, nicht aber im Wirkstoff (API) selbst, NDMA nachgewiesen wurde. Das deckt sich mit den Einschätzungen von Helmut Buschmann, Fritz Sörgel und Ulrike Holzgrabe aus der DAZ 51/2019: „Ein Blick auf die chemische Struktur des Metformins zeigt, dass es aber auch zu einer nachträglichen Bildung von Nitrosamin während der Lagerung im Fertigarzneimittel kommen kann“, heißt es dort. Zu den aktuellen Meldungen, dass das NDMA aus dem Blister kommen könnte, heißt es: Es sei ebenfalls davon auszugehen, dass unterschiedliche physikochemische Eigenschaften, die die Diffusion von Wasser und Sauerstoff von der Umgebung in den Blister-Raum bestimmen, einen signifikanten Einfluss haben – sodass es unter bestimmten Lagerbedingungen in Abhängigkeit vom Blistermaterial zu unterschiedlichen Zersetzungskinetiken kommen könne.
Auch beim mit NDMA verunreinigten Wirkstoff Ranitidin, wird diskutiert, dass das Nitrosamin (teils) erst während der Lagerung entsteht.
Drohen Metformin-Engpässe in der EU?
Bedeutet das nun auch eine gewisse „Entwarnung“ für Europa? Im Metformin von Firmen wie Heritage, Ingenus Pharmaceuticals, Sun Pharma, Westminster Pharmaceuticals, Aurobindo und Major Pharmaceuticals wurde von der FDA immerhin kein NDMA nachgewiesen. Was das für europäische Unternehmen bedeutet bleibt dabei zunächst offen. Allerdings verrät ein Blick auf die Seite des EDQM (European Directorate for the Quality of Medicines), dass es zumindest eine gewisse Parallele geben könnte. So hat Sun Pharmaceutical Industries Ltd. aus Mumbai (Indien) offenbar erst am 7. Januar 2020 sein CEP-Zertifikat für Metformin selbst zurückgezogen. (So ein Zertifikat besagt, dass die Prüfung nach Arzneibuch ausreicht.) Auch ein Wirkstoffhersteller aus Italien – dessen Name in der Liste der FDA nicht auftaucht – hat am 7. Januar sein CEP-Zertifikat zurückgezogen. Nur ein Zufall?
Mehr zum Thema

Umsetzung des GSAV
Wo bleiben die öffentlichen Informationen über Wirkstoffhersteller?
Zumindest für Deutschland gibt es seit dem vergangenen Montag offiziell einen Lieferengpass bei Metformin von Zentiva zu verzeichnen: In der Lieferengpassliste des BfArMs steht ganz klar und deutlich als Grund für den Lieferengpass: „Fertige Chargen von Metformin sind von uns zur Zeit gesperrt, da diese auf NDMA untersucht werden.“ Ein Ende des Engpasses wird für März 2020 erwartet.



























3 Kommentare
Zersetzung
von Joachim Sievers am 06.02.2020 um 10:31 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Einnahme von Metformin Licht
von Silvia Linzert am 06.02.2020 um 4:47 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Einnahme von Metformin Licht
von DAZ.online am 06.02.2020 um 9:33 Uhr
Das Kommentieren ist aktuell nicht möglich.