
- DAZ.online
- News
- Pharmazie
- „Ranitidin bildet ...
US-Online-Apotheke Valisure
„Ranitidin bildet tausende von Nanogramm NDMA im Magen“
Stuttgart - 19.09.2019, 12:44 Uhr

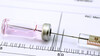
Während sich im Fall um mit Nitrosaminen verunreinigte Sartane schon einiges geklärt hat, beginnen die Arzneimittelbehörden gerade erst die Puzzle-Teile der „Operation Ranitidin“ zusammenzusetzen. Es gibt Hinweise, dass das Antazidum ausgerechnet im Magen NDMA bilden soll. (Foto: sakramir / stock.adobe.com)
Aus dem Valsartan-Skandal des Sommers 2018 ist mittlerweile ein Sartan-Skandal (mit Tetrazolring-Struktur) geworden. Schnell deutete sich zudem an, dass neben den Blutdrucksenkern weitere Wirkstoffe mit Nitrosaminen verunreinigt sein könnten. Im großen Stile bestätigt hat sich dieser Verdacht vergangenen Dienstag mit den Ranitidin-Rückrufen. Und so ist aus dem Valsartan-Skandal mittlerweile ein Nitrosamin-Skandal geworden. Doch wie kommt das Nitrosamin NDMA ins Ranitidin? Die Ursachen im Fall Valsartan scheinen sich nicht einfach auf Ranitidin übertragen zu lassen.
DAZ.online berichtete bereits am Dienstagmorgen, dass die Online-Apotheke „Valisure“ eigenen Angaben zufolge den entscheidenden Hinweis auf das Nitrosamin NDMA in Ranitidin an die Arzneimittelbehörden geliefert hatte. So kam es, dass vergangenen Freitag sowohl die US-amerikanische (FDA) als auch die europäische Arzneimittelbehörde (EMA) bekannt gaben, das H₂-Antihistaminikum Ranitidin (ein Antazidum) näher auf Nitrosaminverunreinigungen zu untersuchen. Das durch die Verunreinigung entstehende Risiko für Patienten soll noch bewertet werden. Zum Ausmaß der Verunreinigung äußerten sich die Behörden nicht näher. Die FDA sprach jedoch von „geringen Mengen“.
Mehr zum Thema

3 mg NDMA in Zantac?
Ranitidin: US-Online-Apotheke gab entscheidenden Nitrosamin-Hinweis

FDA und EMA informieren
Nitrosamin-Verunreinigungen: NDMA in Ranitidin gefunden
Ganz anders die US-Online-Apotheke Valisure mit angeschlossenem Labor, die damit wirbt, die einzige Apotheke zu sein, die jede Charge jedes Arzneimittels, das sie verkauft, selbst testet. Sie will bis zu 3 mg NDMA in Ranitidin gefunden haben. Wie genau Valisure auf NDMA in Ranitidin gestoßen ist, hat die Apotheke noch am Dienstag auf ihrem Internetauftritt veröffentlicht.
Was dort zunächst ins Auge sticht: Während die Pressemitteilungen der EMA, der FDA und des BfArM nahelegen, dass Ranitidin mit NDMA „verunreinigt“ sein kann – erste Rückrufe sind bereits erfolgt –, deutet schon die Gesamtübersicht der Ranitidin-Untersuchung von Valisure an, dass es sich um keine Verunreinigung im eigentlichen Sinne, sondern vielmehr um ein Abbauprodukt von Ranitidin handelt, das sich wiederum erst im Körper bildet.
Sollten die Behörden dies bestätigen, wäre NDMA – anders als im Fall der Sartane – kein Problem, das erst seit einigen Jahren besteht, sondern seit es Ranitidin gibt: In den USA soll es bereits eine Sammelklage gegen die Zulassungsinhaber von Zantac® geben, die die These aufstellt, dass die Gefahren um Ranitidin bereits seit 40 Jahren bekannt sind.
Mehr zum Thema

Teil 1: Nur die Spitze des Eisbergs?
Sartan-Skandal: FDA verhängt Importverbot gegen Lösungsmittelhersteller
Als Hauptursache der NDMA-Verunreinigung im Fall Valsartan des Sommers 2018 hingegen wurde lange Zeit die Änderung der Wirkstoffsynthese im Jahr 2012 als Hauptursache angenommen. Mittlerweile ist aber auch die Problematik um verunreinigte Lösungsmittel immer weiter in den Fokus gerückt.
Dass das Lösungsmittel auch im Fall Ranitidin eine Rolle spielen könnte, lässt sich nicht ausschließen. Die Ausführungen von Valisure stellen jedoch eine andere Theorie auf.
Wie kommt NDMA in eine Ranitidin-Tablette?
Laut Valisure ist der Wirkstoff Ranitidin instabil und kann Millionen von Nanogramm NDMA bilden. Auch eine wissenschaftliche Arbeit, die im November 2018 veröffentlicht wurde („NDMA impurity in valsartan and other pharmaceutical products: Analytical methods for the determination of N-nitrosamines“), spekuliert, dass die Exposition des Wirkstoffs Ranitidin gegenüber Luft und Licht zur Bildung von NDMA während der Lagerung führen könnte.
Valisure führt an, dass Ranitidin bereits seit den 1980er Jahren im Verdacht steht, durch Reaktion mit Nitrit im Magen NDMA zu bilden. Um das Jahr 2000 herum sollen Studien dann die Instabilität von Ranitidin gezeigt haben. Seine Dimethylamin-Gruppe (DMA) wurde unter oxidativen Bedingungen mit der Bildung von NDMA in Verbindung gebracht. 2019 will Valisure dann selbst gezeigt haben, dass Ranitidin NDMA bilden kann, indem es mit sich selbst reagiert. Ranitidin sei sowohl der Lieferant für Nitrit als auch für DMA.
Was mit einer Ranitidin-Tablette im Körper passiert
Zusätzlich zur eigenen Instabilität soll Ranitidin NDMA im menschlichen Körper generieren können. So soll in den 1980er Jahren gezeigt worden sein, dass Ranitidin tausende von Nanogramm NDMA unter Bedingungen bilden kann, wie sie im menschlichen Magen anzutreffen sind. Eine Studie der Universität Stanford soll im Jahr 2016 wiederum den Verdacht aufgestellt haben, dass sich sogar Millionen an Nanogramm NDMA im menschlichen Körper außerhalb des Magens aus Ranitidin bilden können – allerdings konnte der Mechanismus nicht erklärt werden.
2019 will Valisure nun ein Enzym (DDAH-1) identifiziert haben, das die weitere Bildung von NDMA im Körper, außerhalb des Magens, erklären könnte.
Wie NDMA in den Urin kommt
Wie DAZ.online bereits berichtete, ist NDMA auch ein Problem bei der Wasseraufbereitung. Valisure führt Daten um das Jahr 2000 an, die zeigen sollen, dass Ranitidin – ausgeschieden über den Urin – als NDMA-Quelle im Trinkwasser verdächtigt wird.
Außerdem hat die Studie der Stanford University aus dem Jahr 2016 auch den Urin von zehn Probanden untersucht, die zuvor eine Standarddosis (150 mg) Ranitidin eingenommen hatten. Das mit dem Urin ausgeschiedene NDMA soll sich in 24 Stunden von 110 auf über 40.000 ng erhöht haben. Zur Erinnerung: Die vorübergehend tolerierte tägliche Aufnahmemenge für NDMA in Sartanen beträgt pro Tag lediglich 96 ng.
130 °C: NDMA bildet sich auch während der Analyse
All diese Faktoren sollen, wie aus der Übersicht von Valisure hervorgeht, zu Tumoren führen können: 2004 soll das „National Cancer Institute“ (NCI) in einer Studie die Antazida Ranitidin und Cimetidin mit Blasenkrebs in Verbindung gebracht haben. Doch es gibt noch weitere Details zur Untersuchung von Valisure, die aus der Übersicht nicht hervorgehen:
Valisure gibt an, zunächst eine durch die FDA empfohlene Analyse-Methode für die Bestimmung von NDMA benutzt zu haben. Das Problem dabei: Die Probe wird 15 Minuten lang auf 130 °C erhitzt, was zur Bildung von NDMA aus Ranitidin in hohen Mengen führte – bis zu rund 3 mg. Deshalb entschied man sich für eine zusätzliche Methode unter Bedingungen, wie sie im menschlichen Körper vorkommen (37 °C). Damit verschob sich die untere Nachweisgrenze von 25 ng auf 100 ng. Zusätzlich wurde den Proben in verschiedenen Konzentrationen Natriumnitrit zugesetzt, wie es auch durch Nahrung in den Magen gelangen könnte. Ab 25 mM Natriumnitrit seien pro Tablette 23.600 ng NDMA nachgewiesen worden. Bei 50 mM Natriumnitrit waren es 304.500 ng NDMA.
Mehr zum Thema
Nitrosamin-Verunreinigungen
Sartane: Risikobewertungsverfahren ist abgeschlossen
Zusätzlich sollen Antazida durch die pH-Erhöhung im Magen das Wachstum nitrat-reduzierender Bakterien im Magen erhöhen, was wiederum die Nitrit-Konzentration im Magen unabhängig von der Nahrung erhöhen könnte.
Andere Antazida scheinen frei von NDMA zu sein
Weil die Instabilität von Ranitidin einzigartig zu sein scheint, gibt es laut Valisure viele alternative Antazida, die eingesetzt werden können – und auch von Valisure auf NDMA getestet wurden: In Cimetidin, Famotidin, Omeprazol, Esomeprazol, Lansoprazol, Pantoprazol, Rabeprazol und Dexlansoprazol wurde kein NDMA gemessen. Neben Ranitidin wurde nur in Nizatidin NDMA-Konzentrationen um 41.000 ng gemessen, was an der ähnlichen Struktur liegen soll.
In Anbetracht dieser Tatsachen hat Valisure die FDA unter anderem dazu aufgefordert, den Verkauf aller Produkte, die Ranitidin enthalten, auszusetzen. Zudem hat sich Valisure auch an die WHO und IARC gewandt, mit der Bitte, das kanzerogene Risiko von Ranitidin einzustufen. Zusätzlich rät Valisure, Ranitidin so zu entsorgen, dass NDMA nicht durch Wiederaufbereitung ins Trinkwasser gelangen kann.





























2 Kommentare
Nitrosamine
von Jürgen am 24.09.2019 um 14:00 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Ergebnisse der Stanford University nie geprüft worden?
von P.D. am 23.09.2019 um 13:04 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.