
- DAZ.online
- News
- Pharmazie
- Neue EU-Medizinprodukte-...
MDR
Neue EU-Medizinprodukte-Verordnung: Was ändert sich für Apotheken?
Berlin - 24.05.2019, 16:15 Uhr

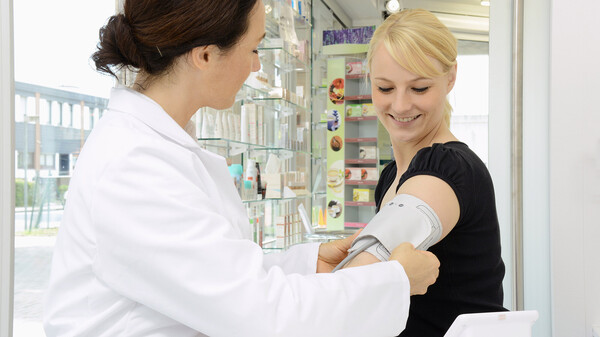
Ist das Medizinprodukt korrekt gekennzeichnet? Mit der neuen Medizinprodukte-Verordnung kommen auf Apotheken demnächst neue Prüf- und Dokumentationspflichten zu. (s / Foto: imago images / blickwinkel)
Vor zwei Jahren ist die neue europäische „Medical Device Regulation“ (MDR) in Kraft getreten. Die nationale Übergangsfrist endet am 26. Mai 2020. Die neue Verordnung sieht unter anderem neue Melde- und Dokumentationspflichten für Apotheken zu Medizinprodukten vor. Außerdem sollen Medizinprodukte mit Verifizierungsmerkmalen, ähnlich wie bei Securpharm, ausgestattet werden.
Auch wenn noch ein Jahr Zeit ist, bis die EU-Medizinprodukte-Verordnung* umgesetzt sein muss: Die Erfahrungen mit der EU-Datenschutzgrundverordnung und der Fälschungsschutzrichtlinie zeigen, dass es nicht schadet, sich ein wenig vor der Deadline mit den Regeln zu befassen.
Die sogenannte Medical Device Regulation (MDR) wurde bereits am 5. Mai 2017 im Amtsblatt veröffentlicht und trat am 25. Mai 2017, zeitgleich zur Verordnung für In-vitro-Diagnostika, in Kraft. Am 26. Mai 2020 läuft die nationale Übergangsfrist der MDR ab.
Medizinprodukte-Verifizierung mit UDI
Durch die MDR erhöht sich vor allem der Aufwand für Hersteller von Medizinprodukten. Weitere Neuerungen sind das „System der einmaligen Produktnummer“ (UDI-Unique Device Identification), das ähnlich wie Securpharm funktionieren soll, sowie die neue europaweite Datenbank Eudamed, in der alle in der EU vermarkteten Medizinprodukte registriert werden sollen.
Aber auch Händler, zu denen die Apotheken ja gehören, sind betroffen. Was die MDR für den Apothekenalltag nach dem 26. Mai 2020 bedeuten könnte, stellte Diplom-Ingenieur Thomas Ertner, der unter anderem die Bundesapothekerkammer berät, vor kurzem auf einer Fortbildung der Apothekerkammer Berlin vor.
Neue Definition von Vorkommnissen
Zum einen ergeben sich für Apotheken neue Melde- und Dokumentationspflichten. Diese entstehen dadurch, dass sich die Definition eines „Vorkommnisses“ mit der MDR ändert. Zwar müssen schon jetzt Vorkommnisse bei Medizinprodukten, ähnlich wie Nebenwirkungen von Arzneimitteln, gemeldet werden. Doch derzeit versteht man unter einem Vorkommnis ein schwerwiegendes Ereignis oder eine Fehlfunktion, die für den Patienten lebensgefährlich sein oder ein Risiko für die öffentliche Gesundheit darstellen könnte. Künftig werden unter dem Begriff Vorkommnis alle unerwünschten Wirkungen beim Patienten sowie jegliche Mängel und Fehlfunktionen des Medizinproduktes subsummiert. Dazu gehört auch eine fehlerhafte Gebrauchsanweisung.
Durch diese erweiterte Definition wird sich die Zahl der Vorkommnismeldungen, die Apotheken an Hersteller und an das Bundesinstitut für Arzneimittel und Medizinprodukte richten müssen, künftig erhöhen. Die schweren Fälle, die derzeit als „Vorkommnis“ eingestuft werden, werden ab dem 26. Mai 2020 als „schwerwiegendes Vorkommnis“ bezeichnet. Außerdem müssen Apotheker über nichtkonforme Medizinprodukte, Beschwerden und Rückrufe ein Register führen und Herstellern Auskunft erteilen, die durch die MDR verpflichtet werden, mögliche Produktrisiken nach Markteinführung zu beobachten.
--------------------------------------------------------------------------------------------------
*Anmerkung der Redaktion: Bei der MDR handelt sich um eine Verordnung und nicht um eine Richtlinie, wie es in der vorherigen Version stand. Wir bitten diesen Fehler zu entschuldigen.
Zehn Jahre Rückverfolgbarkeit
Eine weitere MDR-Vorgabe ist, dass die Rückverfolgbarkeit im Medizinprodukte-Warenverkehr über zehn Jahre gewährleistet sein muss. Apotheken müssen daher die Unterlagen aufbewahren, aus denen hervorgeht, wo das Medizinprodukt bezogen wurde und an welchen Angehörigen der Gesundheitsberufe oder an welche Gesundheitseinrichtung das Produkt abgegeben wurde. Geht das Medizinprodukt direkt an den Patienten, endet die Dokumentationspflicht der Apotheke. Kauft beispielsweise eine Hebamme Nasentropfen mit Kochsalzlösung für das Baby einer ihrer Patientinnen, müssen ihre Daten als Angehörige der Gesundheitsberufe dokumentiert werden. Wenn dieselbe Person die Nasentropfen für ihr eigenes Kind besorgt, ist der Vorgang dagegen nicht dokumentationspflichtig.
„Repräsentative“ Stichproben
Eine weitere neue Verpflichtung ist, dass Apotheken künftig, ähnlich wie bei Fertigarzneimitteln, Stichproben aus ihrem Medizinprodukteportfolio kontrollieren müssen. Dabei hat das pharmazeutische Personal zu überprüfen, ob das Medizinprodukt eine CE-Kennzeichnung inklusive EU-Konformitätserklärung trägt, die Herstellerinformation beiliegen, die Kennzeichnung vorhanden und korrekt ist.
Außerdem muss die Apotheke prüfen, ob der Hersteller eine UDI vergeben hat. Hierzu gibt es Übergangsfristen: Bei Klasse I Medizinprodukte, zu denen die meisten Medizinprodukte in der Apotheke gehören, haben Hersteller bis Mai 2025 Zeit, die UDI anzubringen. Klasse III Medizinprodukte und Implantate müssen bis Mai 2021 verifizierungsfähig sein, bei Klasse II Produkten haben Hersteller bis Mai 2023 Zeit.
Vorsicht beim Umpacken
Weitere Neuerungen betreffen Händler „mit besonderen Tätigkeiten“ also Händler, die Änderungen an Medizinprodukten oder deren Verpackung vornehmen. Hier erhöht sich der Aufwand für Apotheken allerdings erheblich. Denn Apotheken müssen den Hersteller sowie die zuständige Behörde 28 Tage vor der geplanten Abgabe des veränderten Medizinprodukts informieren. Außerdem müssen Produkte, deren Verpackung geändert wurde, mit Namen und Adresse der Apotheke gekennzeichnet und der Vorgang im QMS-Handbuch dokumentiert werden.
Kombiniert die Apotheke unterschiedliche Medizinprodukte in einer neuen Verpackung – ein Beispiel ist das Zusammenstellen von OP-Sets für Praxen, die ambulante Eingriffe durchführen –, bringt die MDR zusätzliche Anforderungen mit sich: Und zwar muss die Apotheke nachweisen, dass die Einzelkomponenten miteinander physikalisch kompatibel sind, auch wenn sie gemeinsam sterilisiert werden. Diese „Beweisführung“ dürfte die Kapazitäten der meisten Apotheken allerdings überschreiten.
Leichter wird es dagegen bei Kompressionsstrümpfen nach Maß. Diese fallen gemäß MDR nicht mehr unter die Kategorie der Sonderanfertigungen, mit denen verstärkte Dokumentationspflichten verbunden sind.
„Marktbereinigung möglich“
Für Inverkehrbringer von Medizinprodukten ist der Mehraufwand, der durch die MDR entsteht, noch größer als für Apotheken. So gibt es Änderungen bei den Klassifizierungsregeln, die überwiegend mit einer Höherklassifizierung verbunden sind. „Dies könnte zu einer Marktbereinigung führen“, prognostiziert Ertner.
Aus Sicht des
Medizinprodukte-Experten tragen die neuen Regelungen zur Patientensicherheit
bei. „Insbesondere die verstärkten Meldepflichten aller Wirtschaftsakteure und
die Verpflichtung zur Nachbeobachtung von Medizinprodukten über den gesamten
Produktlebenszyklus durch die Hersteller bringen künftige Verbesserungen bei
der Sicherheit von Medizinprodukten mit sich“, findet Ertner. Allerdings hat er
Bedenken, ob das Timing für die nationale Umsetzung eingehalten werden kann: „Nach
Informationen des Bundesverbandes Medizintechnik BVMed hat derzeit nur eine
einzige der 57 Benannten Stellen in der EU die Neubenennung für die MDR
abgeschlossen, weniger als die Hälfte konnte bisher auditiert werden. Hinzu kommt,
dass ein Teil der Benannten Stellen ihren Sitz in Großbritannien hat. Für die
zentrale europäische Datenbank Eudamed gibt es noch viele offene Punkte zu
klären, bis diese in der Lage ist, die Aufgaben der MDR zu erfüllen. Der
Umsetzungstermin Ende Mai 2020 wird denkbar knapp werden.“
























10 Kommentare
Medizinprodukte-Verordnung
von Uto Ziehn am 01.12.2019 um 14:33 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Frage von Herrn Thomas Witschel am 04.08.2019
von Dr. Gert Schorn am 06.08.2019 um 16:42 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Auseinzeln
von Christoph am 26.05.2019 um 12:55 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Auseinzeln
von Dr. Gert Schorn am 27.05.2019 um 12:11 Uhr
AW: Auseinzeln
von Dr. Gert Schorn am 27.05.2019 um 12:16 Uhr
Kommentar von Heilo Barz
von Dr. Gert Schorn am 25.05.2019 um 17:33 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Kommentar von Heilo Barz
von Thomas Witschel am 04.08.2019 um 8:43 Uhr
Diktatur der EURO-Richtlinien und Gesetze!
von Heiko Barz am 25.05.2019 um 11:33 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Neues EU-Recht zu Medizinprodukten und In-vitro-Diagnostica
von Dr. Gert Schorn am 24.05.2019 um 22:43 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Neues EU-Recht zu Medizinprodukten und
von Bettina Jung am 27.05.2019 um 9:48 Uhr
Das Kommentieren ist aktuell nicht möglich.