
- DAZ.online
- News
- Pharmazie
- Neue EU-Medizinprodukte-...
MDR
Neue EU-Medizinprodukte-Verordnung: Was ändert sich für Apotheken?
Berlin - 24.05.2019, 16:15 Uhr

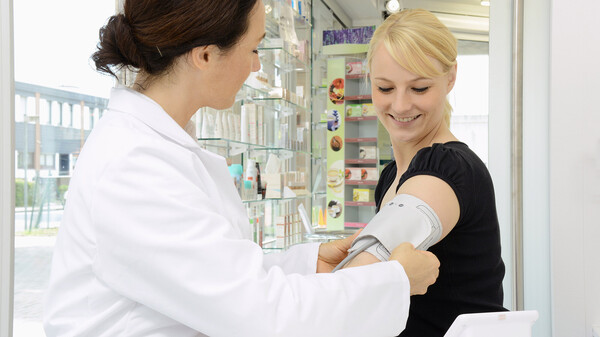
Ist das Medizinprodukt korrekt gekennzeichnet? Mit der neuen Medizinprodukte-Verordnung kommen auf Apotheken demnächst neue Prüf- und Dokumentationspflichten zu. (s / Foto: imago images / blickwinkel)
Zehn Jahre Rückverfolgbarkeit
Eine weitere MDR-Vorgabe ist, dass die Rückverfolgbarkeit im Medizinprodukte-Warenverkehr über zehn Jahre gewährleistet sein muss. Apotheken müssen daher die Unterlagen aufbewahren, aus denen hervorgeht, wo das Medizinprodukt bezogen wurde und an welchen Angehörigen der Gesundheitsberufe oder an welche Gesundheitseinrichtung das Produkt abgegeben wurde. Geht das Medizinprodukt direkt an den Patienten, endet die Dokumentationspflicht der Apotheke. Kauft beispielsweise eine Hebamme Nasentropfen mit Kochsalzlösung für das Baby einer ihrer Patientinnen, müssen ihre Daten als Angehörige der Gesundheitsberufe dokumentiert werden. Wenn dieselbe Person die Nasentropfen für ihr eigenes Kind besorgt, ist der Vorgang dagegen nicht dokumentationspflichtig.
„Repräsentative“ Stichproben
Eine weitere neue Verpflichtung ist, dass Apotheken künftig, ähnlich wie bei Fertigarzneimitteln, Stichproben aus ihrem Medizinprodukteportfolio kontrollieren müssen. Dabei hat das pharmazeutische Personal zu überprüfen, ob das Medizinprodukt eine CE-Kennzeichnung inklusive EU-Konformitätserklärung trägt, die Herstellerinformation beiliegen, die Kennzeichnung vorhanden und korrekt ist.
Außerdem muss die Apotheke prüfen, ob der Hersteller eine UDI vergeben hat. Hierzu gibt es Übergangsfristen: Bei Klasse I Medizinprodukte, zu denen die meisten Medizinprodukte in der Apotheke gehören, haben Hersteller bis Mai 2025 Zeit, die UDI anzubringen. Klasse III Medizinprodukte und Implantate müssen bis Mai 2021 verifizierungsfähig sein, bei Klasse II Produkten haben Hersteller bis Mai 2023 Zeit.























10 Kommentare
Medizinprodukte-Verordnung
von Uto Ziehn am 01.12.2019 um 14:33 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Frage von Herrn Thomas Witschel am 04.08.2019
von Dr. Gert Schorn am 06.08.2019 um 16:42 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Auseinzeln
von Christoph am 26.05.2019 um 12:55 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Auseinzeln
von Dr. Gert Schorn am 27.05.2019 um 12:11 Uhr
AW: Auseinzeln
von Dr. Gert Schorn am 27.05.2019 um 12:16 Uhr
Kommentar von Heilo Barz
von Dr. Gert Schorn am 25.05.2019 um 17:33 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Kommentar von Heilo Barz
von Thomas Witschel am 04.08.2019 um 8:43 Uhr
Diktatur der EURO-Richtlinien und Gesetze!
von Heiko Barz am 25.05.2019 um 11:33 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Neues EU-Recht zu Medizinprodukten und In-vitro-Diagnostica
von Dr. Gert Schorn am 24.05.2019 um 22:43 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Neues EU-Recht zu Medizinprodukten und
von Bettina Jung am 27.05.2019 um 9:48 Uhr
Das Kommentieren ist aktuell nicht möglich.