
- DAZ.online
- News
- Pharmazie
- Zulassungsempfehlung für...
Positives Votum für Flucelvax Tetra
Zulassungsempfehlung für Vierfach-Grippeimpfstoff aus Zellkultur
Stuttgart - 22.10.2018, 12:30 Uhr
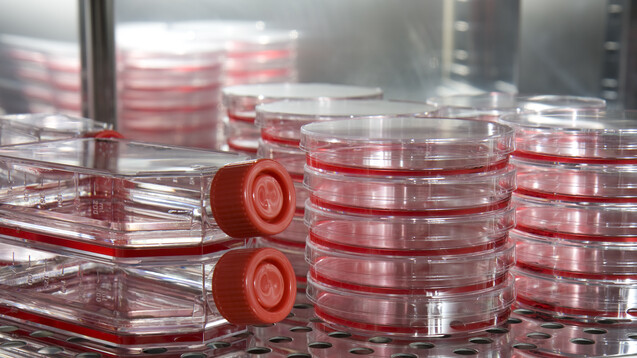
Keine Eier, sondern nur noch Zellen braucht es für den zellbasierten Grippeimpfstoff Flucelvax Tetra. (s / Foto: Sven Hoppe/stock.adobe.com)
Der Humanarzneimittelausschuss der EMA (CHMP) hat einen weiteren Vierfachimpfstoff gegen Grippe zur Zulassung empfohlen. Das Besondere an dem Präparat, das unter dem Namen Flucelvax® Tetra vermarktet werden soll, ist, dass er in Zellkulturen statt in Hühnereiern produziert wird. Eingesetzt werden kann er ab einem Alter von neun Jahren.
Grippeimpfstoffe werden standardmäßig in Hühnereiern produziert. Ein Ei ergibt eine Impfdosis. Im Falle einer Grippepandemie wäre es nicht möglich mit diesem Verfahren kurzfristig außerplanmäßig große Mengen Impfstoff zu produzieren, weil die Vorlaufzeit für die Beschaffung der Eier recht lang ist. Deshalb wird schon lange an zellbasierten Impfstoffen geforscht. Diese hätten zudem den Vorteil, dass sie kein Hühnereiweiß enthalten und somit auch bei Menschen mit schwerer Hühnereiweißallergie eingesetzt werden können. Vor etwas mehr als zehn Jahren erhielt Novartis die Zulassung für einen zellbasierten Grippeimpfstoff – Optaflu®. Dieser setzte sich aber nicht durch, vermutlich auch wegen Sicherheitsbedenken bezüglich einer möglichen Tumorgenität – auch wenn diese vom PEI zerstreut wurden. Optaflu® verschwand schließlich vom Markt. Derzeit gibt es in Deutschland keinen zellbasierten Impfstoff.
Mehr zum Thema
Nun ist die Zeit offenbar reif für einen neuen zellbasierten Grippeimpfstoff, entsprechend dem aktuellen Trend natürlich tetravalent. Vergangene Woche hat der CHMP sich für die Zulassung eines entsprechenden Vakzins ausgesprochen. Flucelvax® Tetra enthält zwei A- und zwei B-Stämme und kann bei Erwachsenen und Kindern ab neun Jahren eingesetzt. Antragsteller ist Seqirus, ein Tochterunternehmen von CSL Behring, das die Grippeimpfstoffdivision von Novartis in Deutschland übernommen hat. Das Unternehmen hatte in den vergangenen Jahren die Dreifachimpfstoffe Afluria® und Begripal® vermarktet sowie Fluad®, einen speziell adjuvantierten Impfstoff für über 65-Jährige. In dieser Saison ist Sequirus in Deutschland nur mit Fluad® auf dem Markt, einen herkömmlich hergestellten Vierfachimpfstoff vertreibt das Unternehmen nicht. In den USA ist Flucelvax® Tetra schon seit 2016 zugelassen. Indiziert ist er dort ab einem Alter von vier Jahren.
Hergestellt wird der Impfstoff in MDCK-Zellen (Madin-Darby canine kidney epithelial cells), also Zellen, die ursprünglich aus Hundenieren isoliert wurden. Das ist dieselbe Zelllinie, in der damals Optaflu® produziert wurde.
Neben dem Grippeimpfstoff empfahl der Ausschuss fünf weitere neue Arzneimittel zur Zulassung, darunter einen Impfstoff gegen Dengue-Fieber (Dengvaxia®) und den Antikörper Lanadelumab (Takhzyro®) zur Prävention von Angioödem-Attacken bei Patienten mit hereditärem Angioödem. Über die Zulassung selbst entscheidet die EU-Kommission. Das Votum des CHMP hat nur Empfehlungscharakter.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.