
- DAZ.online
- News
- Pharmazie
- USA: Importverbot für ...
Valsartan-Hersteller
USA: Importverbot für alle Zhejiang Huahai-Produkte
Stuttgart - 01.10.2018, 13:10 Uhr

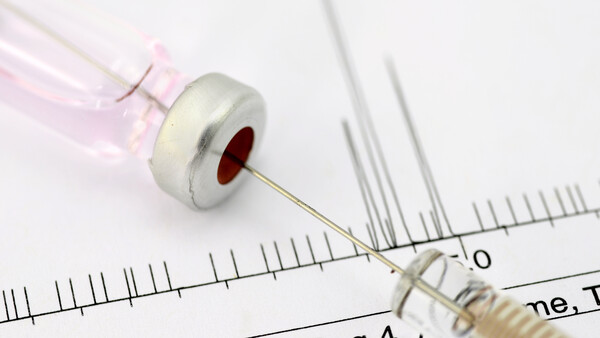
Noch wurde von der EU, wie in den USA, kein generelles Import-Verbot gegen den Valsartan-Hersteller Zhejiang Huahai ausgesprochen. Bislang darf nur Valsartan nicht in die EU. (Foto: Theerawat / stock.adobe.com)
Jetzt also doch: In der Vergangenheit hatten europäische Inspektionen beim Valsartan-Hersteller Zhejiang Huahai in China keine Hinweise auf nicht GMP-konformes Herstellen geliefert. Nun wurde aber ein Bericht der italienischen Arzneimittelbehörde veröffentlicht, demzufolge Zhejiang nicht GMP-konform arbeitet. Der Bericht bezieht sich bislang nur auf die Valsartan-Herstellung. In den USA ist die Arzneimittelbehörde FDA schon einen Schritt weiter und hat vergangenen Freitag ein generelles Importverbot gegen alle Produkte von Zhejiang Huahai verhängt.
Die US-amerikanische Arzneimittelbehörde FDA hatte bereits Mitte September elf neue Mängel-Beobachtungen beim Valsartan-Hersteller Zhejiang Huahai veröffentlicht. Der chinesische Wirkstoffhersteller steht im Mittelpunkt des Falls Valsartan. Von der EU ließen bislang keine Dokumente auf nicht GMP-konformes Arbeiten bei Zhejiang Huahai schließen. Nun wurde am vergangenen Freitag aber auch ein Inspektionsbericht der EU veröffentlicht, der die Valsartan-Produktion von Zhejiang Huahai unter die Lupe genommen hat. Bei dem EU-Bericht handelt es sich nicht nur um eine Dokumentation der bei der Inspektion beobachteten Mängel, wie etwa bei dem 483-Formular der FDA, sondern um einen Non-Compliance-Report, der die Valsartan-Herstellung von Zhejiang Huahai jetzt offiziell als nicht GMP-konform erklärt.
Mehr zum Thema

Dritter Inspektionsbericht der FDA
Elf neue Mängel-Beobachtungen beim Valsartan-Hersteller Zhejiang Huahai

Umstrittener Valsartan-Hersteller
Hamburger Arzneimittelaufsicht inspizierte Zhejiang Huahai regelmäßig

Zhejiang Huahai Pharmaceutical
Die FDA fand schon 2017 eine unbekannte Verunreinigung beim Valsartan-Hersteller
Die Inspektion, auf die sich der europäische Non-Compliance-Bericht bezieht, endete am 13. September 2018 und wurde durch die italienische Arzneimittelbehörde durchgeführt, die von Seiten der EU auch im Dezember 2017 Zhejiang Huahai zuletzt in Chuannan, Linhai inspiziert hatte. Damals war Valsartan kein Gegenstand der Inspektion – wohl aber die Wirkstoffherstellung von Olmesartan und Losartan. Dort schien damals alles GMP-konform zu sein, was mit einem entsprechenden Zertifikat bestätigt wurde.
Die neueste europäische Inspektion soll nun gemeinsam von der EMA und der EU-Arzneimittelbehörde EDQM anlässlich der NDMA/NDEA-Problematik eingeleitet worden sein. Dabei seien neun „wesentliche“ und acht „sonstige“ GMP-Abweichungen festgestellt worden.




























1 Kommentar
ACE Hemmer von Zhejiang Huahai ...
von Kritiker am 01.10.2018 um 15:55 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.