
- DAZ.online
- News
- Pharmazie
- Bei Arixtra klemmt der ...
Apotheker müssen zusätzlich hinweisen
Bei Arixtra klemmt der Nadelschutz
19.07.2017, 16:00 Uhr
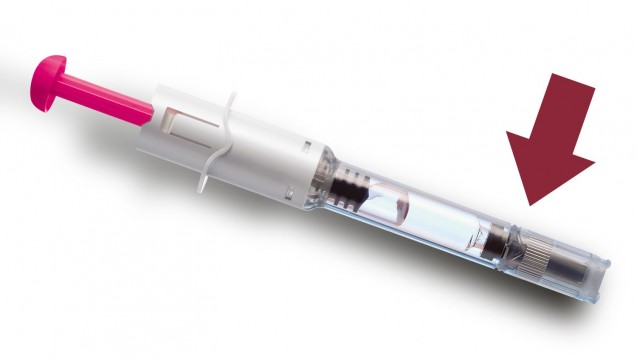
Defekter Nadelschutz bei Arixtra erfordert zusätzliche Beratung durch die Apotheke. (Foto: Aspen Pharma Trading Limited / Bearbeitung JH)
Ein besonders hartnäckiger Nadelschutz führt bei einigen Chargen von Arixtra derzeit zu Problemen. Die betroffenen Chargen waren zunächst gesperrt. Aspen bekam nun aber von der EMA grünes Licht für die Marktfreigabe – trotz des bekannten Defekts. Wie müssen Patienten den Nadelschutz entfernen? Worauf sollten Apotheker ihre Arixtra-Kunden bei den Fondaparinux-Spritzen hinweisen? DAZ.online hat mit dem Stufenplanbeauftragten von Aspen gesprochen.
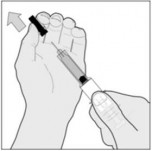
Wie wird der Arixtra Nadelschutz entfernt?
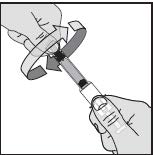
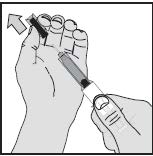
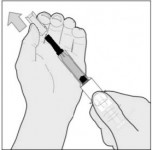
„Bei Abnahme der starren Nadelschutzkappe kann die Nadelschutzhülle bei einigen Spritzen auf der Nadel verbleiben“, schildert Dr. Christoph Buss, Stufenplanbeauftragter von Aspen Pharma Trading Limited, das akute Problem bei Arixtra. „In einem solchen Fall kann die Nadelschutzhülle manuell entfernt werden“, erklärt Buss. Für die gewohnte Anwendung der Thrombosespritzen ist somit bei einigen Arixtra-Chargen ein zweiter Handling-Schritt erforderlich. Darauf sollten Apotheker ihre Arixtra-Kunden aktuell hinweisen, um die sichere Anwendung der Thromboseprophylaxe zu sichern. Wie wird der Nadelschutz manuell entfernt? DAZ.online hat die Beratung zu Arixtra für Sie zusammengestellt.
(Alle Illustr.: Aspen Pharma Trading Limited)
Übersicht der Arixtra-Chargen mit defektem Nadelschutz
Von der besonders festsitzenden Nadelschutzkappe sind nur einige Chargen betroffen. Was also ist in der Produktion schief gelaufen? Und wie gewährt Aspen, dass künftige Chargen wieder einwandfrei funktionieren? DAZ.online hat beim Stufenplanbeauftragten von Aspen nachgefragt.
Betroffen von diesem Defekt sind nur einige Chargen der Stärken Arixtra 2,5 mg/0,5 ml, Arixtra 5 mg/0,4 ml und Arixtra 7,5 mg/0,6 ml und hierbei längst wiederum nicht alle Spritzen dieser Chargen, „aber mehr Spritzen als im Rahmen der Freigabeprüfung zugelassen sind“, erklärt Dr. Christoph Buss. Die Tabelle zeigt eine Übersicht der vom Nadelschutzdefekt betroffenen Arixtra-Chargen.
| Produkt | Packungs-größe | PZN | Betroffene Chargen |
|---|---|---|---|
| Arixtra 2,5 mg/0,5 ml | 7 x 0,5 ml | 02142187 | 0011B |
| Arixtra 2,5 mg/0,5 ml | 10 x 0,5 ml | 02142193 | 0012 |
| Arixtra 2,5 mg/0,5 ml | 20 x 0,5 ml | 02450612 | 0012, 0013A |
| Arixtra 5 mg/0,4 ml | 7 x 0,4 ml | 04191818 | 2006 |
| Arixtra 7,5 mg/0,5 ml | 7 x 0,5 ml | 04191830 | 2007 |
| Arixtra 7,5 mg/0,5 ml | 20 x 0,5 ml | 04191853 | 2006A, 2006B |
EMA gibt Chargen frei – trotz des Defekts. Warum?
„Die betroffenen Chargen wurden in Abstimmung mit den zuständigen Behörden freigegeben, um einen Lieferengpass zu verhindern“, erklärt Buss. „Die Sicherheit und Wirksamkeit des Produktes ist nicht beeinträchtigt“, betont der Stufenplanbeauftragte. Aspen ist der einzige Hersteller des antithrombotischen Wirkstoffs Fondaparinux, dem Wirkstoff in Arixtra. Hergestellt wird das Fertigprodukt in der Herstellstätte Aspen Notre Dame de Bondeville in Frankreich.
Als relativ selektiver Hemmstoff des Blutgerinnungsfaktors X, ist Fondaparinux eine der möglichen Therapieoptionen zur Antikoagulation bei Patienten mit einer heparininduzierten Thrombozytopenie (HIT).
Warum tritt das Problem jetzt auf?
Warum das Problem mit den festsitzenden Nadeln jetzt neu auftritt und sich der Nadelschutz seither einwandfrei entfernen ließ, kann sich Aspen nicht richtig erklären. Man habe in der Produktion nichts umgestellt. „Ursache für den Defekt ist eine erhöhte Ablösekraft des Nadelschutzes in Verbindung mit einer verringerten Rückhaltekraft der Klammer". Dies könnten durch geringfügige, eventuell thermisch bedingte, Fehlformungen der fixierenden Klammer verursacht werden.
Einzeln betrachtet seien beide Abweichungen innerhalb der vorgegebenen Spezifikation gewesen. Letztlich potenzierte sich das Zusammenspiel – äußerer Nadelschutz und rückhaltende Klammer – hier wohl negativ.
Wie vermeidet Aspen künftig defekte Arixtra-Spritzen?
„Wir haben das Design umgestellt, dass der Defekt künftig nicht wieder auftritt“, sagt Dr. Christoph Buss. Diese Umstellung erfordere allerdings auch regulatorische Maßnahmen und Schritte, ergänzt der Stufenplanbeauftragte. „Die Maßnahmen zur Korrektur und Vorbeugung sind in Abstimmung mit den zuständigen Behörden in Umsetzung", allerdings könne der Zeitpunkt, bis diese Maßnahmen endgültig umgesetzt sind, nicht definitiv vorausgesagt werden. Bis dahin wird es also weiterhin Arixtra-Spritzen mit defektem Nadelschutz geben, im deutschen Markt aber auch in weiteren europäischen Ländern.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.