
- DAZ.online
- News
- Zertifizierungsengpass ...
Stoffliche Medizinprodukte
Zertifizierungsengpass bei Meerwassernasensprays und Co. befürchtet
Bonn - 25.01.2017, 16:00 Uhr

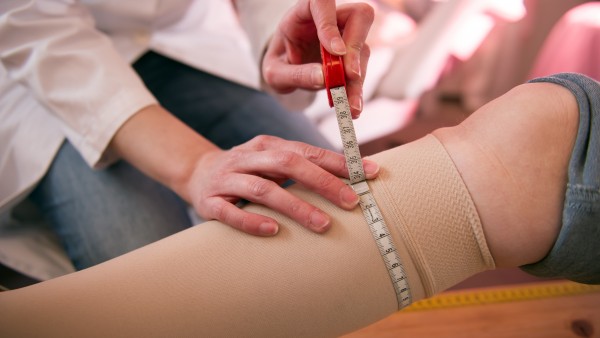
Auch salzhaltige Nasensprays sind sogenannte stoffliche Medizinprodukte, die zertifiziert werden müssen. (Foto: arborpulchra / Fotolia)
Schwund bei den Benannten Stellen
Genau hier hakt der BAH nun mit seiner Befürchtung, die bei der heutigen Informationsveranstaltung laut wurde, ein. Für die Benannten Stellen werden die Karten nach der neuen EU-Verordnung ebenfalls neu gemischt. Sie müssen sich in einem Übergangsprozess neu benennen lassen. Wie viele dabei auf der Strecke bleiben, halten Experten für ungewiss. Nach Angaben des BAH waren bis 2012 europaweit circa 80 Benannte Stellen für Medizinprodukte benannt (notifiziert). Als Reaktion auf den Skandal um verunreinigte Brustimplantate (PIP-Skandal) beschloss die EU-Kommission ein Paket mit Sofortmaßnahmen, mit dem unter anderem die Benennung der zuständigen Stellen insbesondere in Hinblick auf deren Kompetenz überprüft wurde. Infolgedessen ging die Anzahl der Benannten Stellen bereits erheblich zurück, sodass derzeit europaweit nur noch rund 50 Benannte Stellen für Medizinprodukte existieren. In Deutschland sind es laut BAH nur noch zehn. Ein weiterer Rückgang könnte besonders die stofflichen Medizinprodukte treffen.
Zertifizierung unrentabel
„Wir befürchten, dass insbesondere die Hersteller stofflicher Medizinprodukte auf der Streichliste vieler verbleibender Benannter Stellen stehen“, sagt Elmar Kroth, Geschäftsführer Wissenschaft des BAH. „Denn einigen Benannte Stellen erachten die Zertifizierung stofflicher Medizinprodukte aufgrund des als ungünstig eingeschätzten Kosten-Nutzen-Verhältnisses als unrentabel.“ Sollte dies dazu führen, dass Hersteller keine Benannte Stelle finden, die ihre Produkte zertifiziert, oder aktuelle Verträge nicht verlängert werden, sei die weitere Verfügbarkeit vieler Produkte fraglich. Benannte Stellen dürften nicht zum Flaschenhals für stoffliche Medizinprodukte werden, sonst sei die Patientenversorgung in Gefahr, ergänzte Kroth.
Die neue EU-Verordnung über Medizinprodukte (MDR) wird voraussichtlich Mitte 2017 in Kraft treten und nach einer Übergangsfrist von drei Jahren in allen EU-Mitgliedstaaten direkt anzuwenden sein


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.