
- DAZ.online
- News
- DAP bietet PZN-Liste ...
Ruhende Zulassungen
DAP bietet PZN-Liste betroffener Präparate
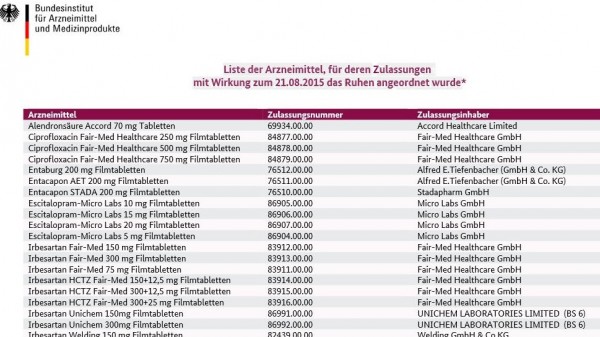
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hat das Ruhen einer Reihe von Zulassungen angeordnet, denen mutmaßlich gefälschte klinische Studien der Firma GVK Biosciences in Indien zugrunde liegen. In den Apotheken und im Großhandel sorgt dies derzeit für viel Verwirrung. Die Software zeigt nicht an, welche Präparate betroffen sind, also nicht mehr vertrieben werden dürfen. Das DeutscheApothekenPortal (DAP) bietet nun Hilfe: Es hat eine PZN-Liste der betroffenen Arzneimittel zusammengestellt.
Die vom BfArM veröffentlichte Liste der betroffenen Arzneimittel ist in der Apothekenpraxis wenig praktikabel. Dabei ist die Sorge groß, falsch abzugeben. Insbesondere, weil sich Rabattarzneimittel unter den betroffenen Präparaten befinden. Beispielsweise haben viele großen Kassen für verschiedene Dosierungen von Irbesartan und Irbesartan/HCT Rabattverträge mit der Firma Heumann, etwa die AOK und die Barmer GEK.
Aber ob die Rabattverträge wirklich betroffen sind, ist auch vielen Krankenkassen noch nicht klar – nicht jeder Vertrag fällt unter die explizit aufgezählten Zulassungen. Bei der Techniker Krankenkasse ist man mittlerweile sicher: Bei ihr ist kein Rabatt-Arzneimittel betroffen. Bei der Barmer GEK prüft man noch, erklärt aber: Soweit die auf der BfArM-Liste genannten Zulassungen mit den Rabattverträgen übereinstimmen, gibt es immer noch ein oder auch zwei Ausweich-Rabattpartner.
Software: Keine schnelle Aufnahme der Änderungen in Sicht
Klar ist: Die nicht mehr verkehrsfähigen Arzneimittel, gleich ob sie rabattiert sind oder nicht, müssen nach den Vorgaben der Apothekenbetriebsordnung in der Apotheke separiert und dürfen nicht mehr abgegeben werden. Doch Informationen über die konkret betroffenen Produkte fehlen den Apotheken. Es wird auch noch etwas dauern, bis die Apotheken-Software die Präparate abbildet. Denn die Informationsstelle für Arzneispezialitäten (IFA) meldet die von den pharmazeutischen Unternehmen angegebenen Neuaufnahmen und Änderungen jeweils zum 1. und 15. des Monats. Diese Daten übernehmen die Softwarehäuser in die Apothekensoftware. Angesichts des regulären Meldeschlusses bei der IFA für Artikeländerungen, ist nicht damit zu rechnen, dass Informationen zu Präparaten, deren Zulassung aufgrund der mangelhaften Arzneimittelstudien von GVK Bio ruht, zeitnah in der Apothekensoftware auftauchen werden: Änderungen, die zum 1. Januar 2015 veröffentlicht werden, konnten bis zum 5. Dezember gemeldet werden. Zu diesem Zeitpunkt hatte das BfArM die entsprechenden Bescheide allerdings noch nicht verschickt. Demnach ist der nächste Termin zur Veröffentlichung der 15. Januar 2015, wofür der Meldeschluss am 18. Dezember abläuft. Bedenkt man, dass einige Unternehmen Widerspruch gegen die BfArM-Bescheide eingelegt haben, ist fraglich, ob und wann die Hersteller das Ruhen der Zulassung melden.
Die nun vom DAP zusammengestellte PZN-Liste (Stand: 10.12 2014) auf Grundlage der vom BfArM veröffentlichten Zulassungsnummern mit entsprechenden Rabattverträgen (falls vorhanden) soll bei der Arbeit helfen.


























Berlin - 12.12.2014, 08:48 Uhr